 固体药品取用
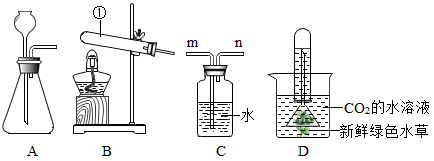
B .
固体药品取用
B .  加热液体
C .
加热液体
C .  检查装置气密性
D .
检查装置气密性
D .  过滤
过滤

选项 | 实验目的 | 实验方案 |
A | 区分O2和N2 | 将带火星的木条伸入集气瓶 |
B | 除去CO2中混有的CO | 将混合气体通入O2中并点燃 |
C | 除去MnO2中的KCl | 将固体溶于水后过滤、洗涤、干燥 |
D | 比较Ag与Cu的活泼性 | 把洁净铜丝放入AgNO3溶液中 |

A.①Ca(OH)2 ②Na2CO3 B.①Na2CO3 ②Ca(OH)2
C.①KOH ②Na2CO3 D.①NaOH ②Na2CO3
【分析、作出猜想】
根据燃烧条件分析:①脱脂棉是物;②吹出的气体可能与Na2O2反应生成了氧气;③反应放出热量,使温度达到脱脂棉的。
在如图装置中,向装有Na2O2的试管中不断吹气,观察到Na2O2粉末由淡黄色逐渐变成白色,在导管口P处放置带火星的木条,木条复燃,证明②成立。同时还观察到U形管中的液面,说明③成立。

【得出结论】
吹出的气体与Na2O2粉末反应生成了O2 , 放出了热量,满足脱脂棉燃烧的条件。
【查阅资料】
①吹出的气体主要成分有氮气、二氧化碳和水蒸气;
②Na2O2粉末不与氮气反应;
③氢氧化钡【Ba(OH)2】可溶于水,氢氧化钙【Ca(OH)2】微溶于水;
④氯化钡(BaCl2)、氯化钙(CaCl2)溶液呈中性。
【作出猜想及推断】
猜想1:固体成分是Na2CO3 , 则CO2参加反应;
猜想2:固体成分是NaOH,则H2O参加反应;
猜想3:固体成分是Na2CO3和NaOH,则CO2和H2O均参加反应。
【实验验证】
实验步骤 | 实验现象 | 分析与结论 |
①取残留白色固体配成溶液,向其中加入过量的氯化钡溶液,振荡,静置 | 白色固体中含有碳酸钠 | |
②取适量步骤①的上层清液,滴加少量酚酞溶液 | 溶液变红色 | 白色固体中含有 |
请写出Na2O2与CO2或H2O反应的化学方程式:(写一个)。