选项 | 素质教育 | 化学知识或原理 |
A | 音乐:“音乐焰火”创造出火树银花不夜天 | 焰色反应属于化学变化 |
B | 体育:北京冬奥会火炬外壳材料是由高性能树脂与碳纤维融合而成的复合材料 | 该复合材料具有耐高温、耐腐蚀等优良的特性 |
C | 美术:宋代《千里江山图》中的绿色来自孔雀石颜料[主要成分为Cu(OH)2·CuCO3],青色来自蓝铜矿颜料[主要成分为Cu(OH)2·2CuCO3] | 孔雀石、蓝铜矿颜料不易被空气氧化且耐酸、耐碱 |
D | 文学:爆竹声中一岁除,春风送暖入屠苏 | 传统爆炸粉为黑火药,其主要成分为木炭、硫磺、KClO3 |
 D .
D . 
A | B | C | D | |
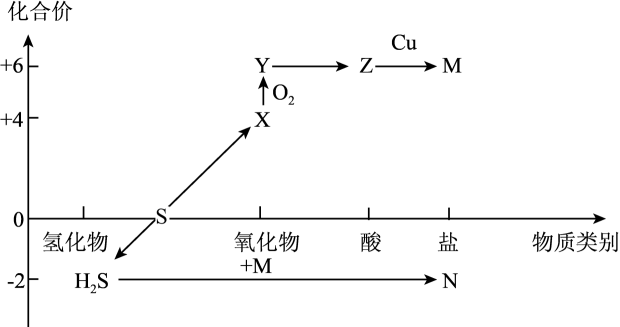
X 中试剂 | 浓盐酸 | 浓硫酸 | 双氧水 | 浓氨水 |
Y 中试剂 | MnO2 | C2H5OH | MnO2 | NaOH |
气体 | Cl2 | C2H4 | O2 | NH3 |
选项 | 劳动项目 | 化学知识 |
A | AgBr用来制作照相胶片 | AgBr见光易分解 |
B | NaCl的溶解度随温度变化不大 | 在盐田中晾晒海水,得到粗盐 |
C | 利用含小苏打的发酵粉烘焙蛋糕 | 小苏打是碳酸氢钠 |
D | SiO2制作光导纤维 | SiO2导电 |

 加热熔融的氢氧化钠固体
B .
加热熔融的氢氧化钠固体
B .  吸收CO2中的HCl杂质
C .
吸收CO2中的HCl杂质
C .  吸收尾气中的Cl2
吸收尾气中的Cl2







编号 | Na2SO4溶液 | AgNO3溶液 | 现象 | |||
体积 mL | 浓度 mol·L−1 | 体积 滴 | 浓度 mol·L−1 | 混合后Ag+浓度mol·L−1 | ||
① | 1 | 1 | 3 | 2 | 0.2 | 出现大量白色沉淀 |
② | 1 | 1 | 3 | 0.5 | 0.05 | 出现少量白色沉淀 |
③ | 1 | 1 | 3 | 0.1 | 0.01 | 有些许浑浊 |
④ | 1 | 1 | 3 | 0.01 | 0.001 | 无明显变化 |
实验一中产生沉淀的离子方程式为。
实验一中编号④无明显变化,若要产生浑浊,溶液中c(SO)理论上至少达到mol·L−1。若向l mL某浓度的NaCl与Na2SO4混合溶液中加入3滴0.1mol·L−1AgNO3溶液,分析上面数据,判断下列说法正确的是(填字母序号)。
A.混合液中c(SO)=1mol·L−1时不会产生Ag2SO4沉淀
B.混合液中c(SO)=0.1 mol·L−1时不会产生Ag2SO4沉淀
C.无论SO浓度大小都会产生Ag2SO4沉淀
D.若使用0.01 mol·L−1AgNO3溶液,可基本排除SO对Cl-检验构成的干扰
实验二:
编号 | AgNO3浓度/mol·L−1 | 现象 | 滴加硝酸后的现象 |
① | 2 | 出现大量白色沉淀 | 滴加稀硝酸,沉淀大量溶解;改加浓硝酸,沉淀较快消失 |
② | 0.5 | 出现少量白色沉淀 | 滴加稀硝酸,沉淀基本消失 |
对于Ag2SO4溶于硝酸的原因提出了如下假设,请完成假设二。
假设一:NO对Ag2SO4溶解起作用。
假设二:。
编号 | 操作 | 现象 | 结论 |
① | 取少量Ag2SO4于试管中,加入2mL水,振荡 | 固体不溶解 | |
② | 将①的浊液分成两等份 | ||
③ | 向其中一份加入1mL0.1mol/L的NaNO3 , 振荡 | 假设一不成立 | |
④ | 向另一份加入 | 假设二成立 |

已知:碳酸锂的溶解度(g·L-1)见表。
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
Li2CO3 | 1.54 | 1.43 | 1.33 | 1.25 | 1.17 | 1.08 | 1.01 | 0.85 | 0.72 |
回答下列问题


已知:①CO(g)+H2O(g) HCOOH(g) △H1=−72.6kJ·mol−1
②2CO(g)+O2(g) 2CO2(g) △H2=−566.0kJ·mol−1
则反应③的平衡常数表达式K= , 写出反应③的热化学方程式。
i.СО2(g)+Н2(g) НСООН(g) △H3<0
ii.CO2(g)+H2(g) CO(g)+H2O(g) △H4
刚性密闭容器中CO2(g)和H2(g)按物质的量1:1投料,平衡时HCOOH和CO的选择性随温度变化如图所示。(选择性是指转化成目标产物的反应物在实际消耗的反应物中的占比)

①曲线a随温度升高而下降的原因是;为同时提高CO2的平衡转化率和平衡时HCOOH的选择性,应选择的反应条件为(填标号)。
A. 低温、低压 B.高温、高压 C.高温、低压 D.低温、高压
②240℃时,容器内压强随时间的变化如下表所示:
时间/min | 0 | 20 | 40 | 60 | 80 |
压强/MPa | p0 | 0.91p0 | 0.85p0 | 0.80p0 | 0.80p0 |
反应i的速率可表示为υ=k·p(CO2)·p(H2)(p为气体分压,分压=总压×气体的物质的量分数, k为常数),则反应在60 min时υ=(用含p0、k的式子表示)。
在密闭容器中通入物质的量均为0.2mol的CH4和CO2 , 在一定条件下发生反应CH4(g)+CO2(g) 2CO(g)+2H2(g),CH4的平衡转化率与温度及压强的关系如图所示。

①由如图可知:压强p1p2(填“>”、“<”或“=”)。
②Y点:υ(正)υ(逆)(填“>”、“<”或“=”)。



