 C .
C .  D .
D . 
①Al(OH)3胶体 ②白酒 ③云或雾 ④FeCl3溶液 ⑤淀粉溶液
|
|
|
|
A.乙炔的空间结构模型 | B. | C.反-2-丁烯的结构简式 | D.氨分子的电子式 |


实验编号 | 温度 ℃ | Na2S2O3 | H2SO4 | 加入H2O 的体积/mL | 出现浑浊的时间/s | ||
体积mL | 浓度mol•L-1 | 体积mL | 浓度mol•L-1 | ||||
1 | 20 | 10 | 0.1 | 10 | 0.1 | 0 | 4 |
2 | 20 | 5 | 0.1 | 10 | 0.1 | V | 8 |
3 | 60 | 10 | 0.1 | 10 | 0.1 | 0 | 2 |
下列说法错误的是( )



目的 | 方案设计 | 现象和结论 | |
A | 检验阿司匹林中是否存在水杨酸 | 取样品,加入蒸馏水和乙醇振荡,再加入两滴氯化铁溶液 | 溶液变紫色,说明存在水杨酸 |
B | 检验含氟化钠的牙膏中的 | 向 | 血红色褪去说明含 |
C | 鉴别 | 各取少量固体加水溶解,分别滴加盐酸酸化的 | 溶液变黄色的是 |
D | 检验卧室内空气是否含甲醛 | 用注射器抽取一针管气体慢慢注入盛有酸性高锰酸钾稀溶液的试管中,观察溶液颜色变化 | 溶液不变色,说明空气中不含甲醛 |
步骤 | 操作 | E(甲组) | F(乙组) |
I | 取少量产物,加入稀盐酸 | 溶解、无气泡 | 溶解,有气泡 |
II | 取步骤I中溶液,滴加KSCN溶液 | 溶液变红 | 无明显变化 |
III | 向步骤II溶液中滴加双氧水 | 红色变深 | 溶液变红 |
①根据上述现象,得出实验结论:E为X3O4(X表示形成化合物M的一种元素),F为(填化学式)。
②乙组实验中,步骤III中溶液由无色变红的原因是(用离子方程式表示)。
③通过交流、讨论,有人认为E中除X3O4外还可能含单质X,判断的理由是。
①C2H6(g) CH4(g)+H2(g)+C(s) △H1=+9kJ·mol-1
②C2H4(g)+H2(g) C2H6(g) △H2=-136 kJ·mol-1
③H2(g)+CO2(g) H2O(g)+CO(g) △H3=+41 kJ·mol-1
④CO2(g)+C2H6(g) C2H4(g)+H2O(g)+CO(g) △H4
△H4=,0.1MPa 时向密闭容器中充入CO2和C2H6 , 发生反应④,温度对催化剂K- Fe-Mn/Si 性能的影响如图:

工业生产综合各方面的因素,根据图中的信息判断反应的最佳温度是 ℃。
主反应: CO2(g)+3H2(g)CH3OH(g)+H2O(g) △H <0
副反应: CO2(g)+H2(g) CO(g)+H2O(g) △H>0
将反应物混合气体按进料比n(CO2): n(H2)=1: 3通入反应装置中,选择合适的催化剂,发生上述反应。
不同温度下,CO2的平衡转化率如图①所示,温度高于503K时,CO2 的平衡转化率随温度的升高而增大的原因是。 实际生产中,保持压强不变,相同反应时间内不同温度下CH3OH的产率如图②所示,由图可知,523K时CH3OH的产率最大,可能的原因是。

已知: NH3·H2O的Kb=1.7 ×10-5 , H2CO3的Ka1=4.3 ×10-7 , Ka2 =5.6 ×10-11。工业生产尾气中的CO2捕获技术之一是氨水溶液吸收技术,工艺流程是将烟气冷却至20℃后用氨水吸收过量的CO2。吸收反应的化学反应方程式为,所得溶液离子浓度由大到小的顺序是(不考虑二氧化碳的溶解)。
相关物质性质:
物质名称 | 相对分子质量 | 颜色、状态 | 溶解性 | 沸点/℃ | 毒性 |
苯乙腈 | 117 | 无色油状液体,密度比水大 | 难溶于水,溶于醇 | 233.5 | 有毒 |
氯化苄 | 126.5 | 无色或微黄色的透明液体 | 微溶于水,混溶于乙醇 | 179.4 | 有毒 |
氰化钠 | 49 | 白色结晶颗粒或粉末 | 易溶于水 | 1496 | 剧毒 |
二甲胺 | 45 | 无色气体,高浓度有类似氨的气味 | 易溶于水,溶于乙醇 | 6.9 | 有毒 |
反应原理:![]() (氯化苄)+NaCN
(氯化苄)+NaCN![]() (苯乙腈)+NaCl
(苯乙腈)+NaCl
主要装置:
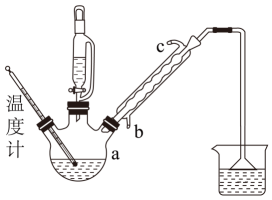
实验步骤:
①向仪器a中加入氯化苄25.3g,缓慢加入适量二甲胺水溶液,放入磁子搅拌。
②安装好球形冷凝管、恒压漏斗及温度计,开启冷凝水,并对仪器a进行加热至90℃。
③向恒压漏斗中加入30%氰化钠水溶液49.0g。
④控制滴加速度与反应温度,使反应在90±5℃下进行。
⑤滴加结束后,加热回流20小时。
⑥反应结束并冷却至室温后,向混合物中加100mL水,洗涤,分液。
⑦往得到的粗产物中加入无水CaCl2颗粒,静置片刻,倒入蒸馏烧瓶中,弃去CaCl2 , 进行减压(2700Pa)蒸馏,收集115~125℃馏分,得到产品无色透明液体22.3g。
回答下列问题:
①能与溶液反应产生
气体
②含有四种化学环境的氢
 的合成路线(其他无机试剂任选)。
的合成路线(其他无机试剂任选)。