 B . 稀释浓硫酸
B . 稀释浓硫酸 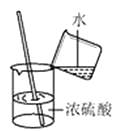 C . 检查气密性
C . 检查气密性  D . 熄灭酒精灯
D . 熄灭酒精灯 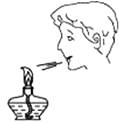
选项 | 实验目的 | 所选试剂及操作 |
A | 除去CO2气体中的CO | 通过足量灼热的氧化铜 |
B | 除去氯化钠溶液中的氯化铜 | 加入过量的氢氧化钠溶液,过滤 |
C | 除去硝酸钙溶液中的硝酸 | 加入过量的碳酸钙,过滤 |
D | 除去氧化钙中的碳酸钙 | 加入适量的盐酸,过滤 |
|
选项 |
X |
Y |
Z |
W |
|
A |
CuO |
CuCl2 |
Cu(OH)2 |
CuSO4 |
|
B |
HCl |
Na2CO3 |
NaOH |
H2O |
|
C |
H2O2 |
O2 |
H2CO3 |
H2O |
|
D |
Ba(OH)2 |
BaCl2 |
Ba(NO3)2 |
BaCO3 |



① 图中表示(填数字)种元素。
② 达到稳定结构原子的是(填序号)。
③ 在化学反应中最容易失去电子的是(填序号)。
④ 元素B与元素E形成化合物的化学式为(用B、E表示)。

根据图示写出反应的化学方程式。
① 组成:电解水实验证明水是由(填元素名称)组成的。
② 结构:水分子中氢、氧原子个数比为。
③ 性质:水能与反应生成碳酸,可用来制备碳酸饮料。
④ 变化:在加热条件下,水能与镁条反应生成氢氧化镁和氢气,试写出该反应的化学方程式。

① 0℃时,三种固体溶解度由大到小的顺序为。
② t2℃时,向100 g水中放入20 g乙物质,所得溶液为(填“饱和”或“不饱和”)溶液。
③ t2℃时,等质量的甲和丙的饱和溶液降温到t1℃,此时,烧杯中所得溶液的溶质质量分数(填“相等”或“不相等”)。
① 若滤液中滴加盐酸,产生白色沉淀,则滤渣中一定含有的固体为。
② 若滤渣中加入稀盐酸,有气体产生,则滤渣中一定含有的固体为。
③ 若得到的滤渣质量与所加锌单质的质量相等,则滤渣成分一共有种组合(填序号)。
A.1种 B.2种 C.3种
④ 写出锌与硝酸银反应的化学方程式。
① 配制1000g 16%的氯化钠溶液,需要量取25%的氯化钠溶液g。
② 配制过程中需要用到的仪器除了量筒、烧杯、胶头滴管、试剂瓶外,还需要。
③ 配置完毕,导致所得溶液溶质质量分数偏大的原因可能是(填序号)。
A.量取水时,采用仰视的方法读数
B.量取25%的氯化钠溶液时,采用仰视的方法读数
C.配制溶液的烧杯内残留有水

