
部分物质在水中的溶解性表(室温)
阴离子 阳离子 | OH﹣ | ||
Ba2+ | 溶 | 不溶 | 不溶 |
Ca2+ | 微溶 | 微溶 | 不溶 |
Mg2+ | 不溶 | 溶 | 微溶 |
①滤纸破损
②液面高于滤纸边缘
③仪器不干净
已知:①部分银盐的溶解性如下表
|
|
NO3- |
Cl- |
CO32- |
|
Ag |
溶 |
不 |
不 |
②氯化银不溶于稀硝酸。
实验Ⅰ、取纯碱样品,加水溶解得溶液X,测得溶液pH约为12。
实验Ⅱ、取溶液X,滴加过量试剂Y,产生能使澄清石灰水变浑浊的气体。
实验Ⅲ、向实验Ⅱ后所得溶液中滴加硝酸银溶液,有白色沉淀生成。
结论:样品中含有氯化钠。
①测定溶液pH的操作:用玻璃棒蘸取溶液滴在pH试纸上,与相比较。
②实验Ⅱ中所加的试剂Y应选用(填字母)。
a、稀盐酸 b、稀硝酸 c、氢氧化钠溶液 d、氯化钙溶液
③由上述实验推断,溶液X中含有的阴离子除Cl-外,还有(填离子符号)。
准确称取2.000g干燥纯碱样品,加水溶解,逐滴加入溶质质量分数为3.65%的稀盐酸,边滴加边搅拌,当两者恰好完全反应时(含碳物质全部转化为CO2),消耗盐酸体积为37.00mL。(该盐酸的密度近似等于1g·mL-1 , 杂质不与盐酸反应)
①通过计算判断该纯碱样品的等级。(写出计算过程)
无水碳酸钠等级规定如下:
|
|
优等品 |
一等品 |
合格品 |
|
碳酸钠质量分数 |
≥99.2% |
≥98.8% |
≥98.0% |
②实验发现,当滴入盐酸体积略少于37.00mL时,溶液pH就降至7以下(约为5),溶液pH小于7的原因是。将此时的溶液煮沸,pH会略有升高,其原因。


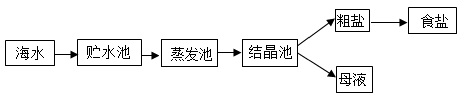
①“蒸发池”中质量逐渐减少的物质是(填化学式)。
②实验室里除去粗盐中难溶性杂质一般步骤为溶解、过滤、蒸发,这三种基本操作中都要使用的玻璃仪器是。
③析出晶体后的“母液”是氯化钠的(选填“饱和溶液”或“不饱和溶液”)。母液中含有MgCl2 , 向母液中加入澄清石灰水有白色沉淀生成,该复分解反应的化学方程式为。
①下列说法正确的是(填字母)。
a.可燃冰和干冰都属于混合物
b.可燃冰与煤相比是较清洁燃料
c.可燃冰和石油都属于可再生能源
②利用CH4和H2O进行催化重整制氢气,反应前后分子变化的微观示意图如图所示。其中“乙→丙”发生反应的化学方程式为。


他们继续向溶液M中滴加碳酸钠溶液,发现只有白色沉淀产生,无其它实验现象。由此可知,溶液M中除了含有酚酞外,还含有的溶质是(填化学式)。
【猜想与假设】甲同学猜想:NaCl、BaCl2
乙同学猜想:NaCl
丙同学猜想:NaCl、Na2CO3
【分析与交流】上述猜想中不合理是同学的猜想。甲同学猜想溶液N中含有NaCl的依据是(用化学方程式表示)。
【实验探究1】用pH试纸测得等浓度的碳酸氢钠溶液的pH为9,碳酸钠溶液的pH为11。
【实验结论1】两者均显碱性,且溶液碱性较强的是 。
【实验探究2】向盛有碳酸钠溶液的烧杯中,逐滴加入一定浓度的稀盐酸并充分搅拌,测得pH变化与时间的关系如图1所示。观察到ab段无气泡产生,从b点开始产生气泡。经测定b点溶质只有碳酸氢钠和氯化钠,c点pH为7。

【实验结论2】碳酸钠和盐酸的反应是分两步发生的,ab段发生反应的化学方程式为 ,c点溶液中的溶质为 。
【查阅资料】①碳酸氢钠受热分解成碳酸钠、水和二氧化碳;②碳酸钠受热不分解。
【实验验证】取一定量的碳酸氢钠放入试管中加热,如图2所示。

【交流反思】试管A管口向下倾斜的原因是 ,试管B中出现 现象,证明有二氧化碳生成。
【实验结论3】碳酸钠的热稳定性强于碳酸氢钠。
【实验方案】
①取少量土壤样品,加蒸馏水充分搅拌,静置澄清后过滤;
②用玻璃棒蘸取少量滤液滴在pH试纸上,等试纸显色后与对比,读出pH,进一步确定土壤酸碱性。
|
|
滤液1 |
滤液2 |
滤液3 |
滤液4 |
|
测得的pH |
5 |
6 |
6 |
5 |
【实验结论】该土地的土壤呈性。
【调查分析】经调查,该土地之前的承包者为使自己种植的农作物生长茂盛,施用了大量化肥——硫酸铵,于是推测土壤的酸碱性出现问题的原因是土壤中含有大量的硫酸铵。
【设计实验】
|
实验步骤 |
实验现象 |
实验结论 |
|
步骤①:取“活动一”中的滤液于试管中,滴加溶液 |
有生成 |
土壤中含有硫酸根离子 |
|
步骤②:另取适量土壤样品,加熟石灰混合研磨 |
有刺激性气味的气体产生 |
土壤中含有离子 |
|
|
所用物质 |
改良原理 |
|
改良酸性土壤 |
熟石灰[Ca(OH)2] |
氢氧化钙能与土壤中的酸性物质反应 |
|
草木灰(主要成分为K2CO3) |
|
|
|
改良碱性土壤 |
硫酸亚铁(FeSO4) |
硫酸亚铁能与土壤中的碱性物质反应 |
【得出结论】兴趣小组的同学们通过分析确定用草木灰改良该土壤。


I组:O2和CO2的实验室制取
任务一:探究废水成分
【参观调查】同学们实地参观了该化工厂,在同技术人员的交谈中得知,车间废水中含有酸性物质。
【猜想假设】该废水中可能含有硫酸和盐酸。
【教师指导】BaSO4、AgCl均为难溶于水的白色沉淀。
|
项目 |
实验步骤 |
实验现象 |
实验结论 |
|
方案 |
①取少量废水于试管中,滴入几滴紫色石蕊溶液 |
|
废水中含有硫酸和盐酸 |
|
②另取少量废水于试管中,滴加过量Ba(NO3)2溶液,静置 |
产生白色沉淀 |
||
|
③取步骤②的上层清液于试管中,滴加几滴 |
产生白色沉淀 |
【反思评价】工厂废水中不含的原因是。
【实验模拟】工厂为同学们提供了100mL废水,在实验室里,同学们模拟工厂中废水净化的方法,设计了如下实验:
①向盛有废水的烧杯中加入将其调节至中性
②再向烧杯中加入少量明矾,用玻璃棒搅拌使之溶解,静置,明矾的作用是。
③将静置后的废水慢慢注入下图所示的废水净化装置中,装置中的X是。

④在过滤后的水中加入少量漂白粉,搅拌,备用。
【小组交流】净化后的废水可再被利用,例如(写1条)。
【成果分享】通过项目化学习,同学们进一步认识到工业生产不仅可为人类创造财富,还可以通过工业化手段推动再生资源的开发和利用。