 检查气密性
B .
检查气密性
B .  测量溶液的pH
C .
测量溶液的pH
C .  取固体药品
D .
取固体药品
D .  熄灭酒精灯
熄灭酒精灯



 B . 探究燃烧的条件与着火点有关
B . 探究燃烧的条件与着火点有关  C . 探究铁生锈与氧气有关
C . 探究铁生锈与氧气有关  D . 利用红磷燃烧测定空气中氧气的含量
D . 利用红磷燃烧测定空气中氧气的含量 
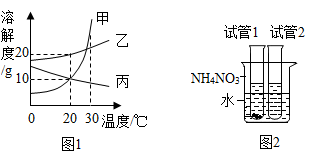
 在一定量的硝酸银和硝酸铜的混合溶液中加入铁粉至过量
B .
在一定量的硝酸银和硝酸铜的混合溶液中加入铁粉至过量
B .  某温度时,向一定量的饱和石灰水中加入少量生石灰
C .
某温度时,向一定量的饱和石灰水中加入少量生石灰
C .  向等质量的镁粉和铁粉中加入稀盐酸至过量
D .
向等质量的镁粉和铁粉中加入稀盐酸至过量
D .  加热一定质量的氯酸钾与二氧化锰混合物
加热一定质量的氯酸钾与二氧化锰混合物
| 选项 | 实验目的 | 实验方案 |
| A | 验证NaOH在空气中部分变质 | 加水充分溶解后,滴加CaCl2溶液 |
| B | 除去NaOH溶液中的Na2CO3杂质 | 滴加适量Ca(OH)2溶液,过滤 |
| C | 除去NaCl晶体中少量KNO3晶体 | 用NaCl饱和溶液洗涤,过滤 |
| D | 验证NaCl中含有H2SO4杂质 | 取样,滴加Ba(NO3)2观察现象 |
A 无机盐 B 油脂 C 糖类 D 水
①可有效缓解全球温室效应 ②可减少对化石燃料的依赖
③该转化过程中发生化学变化 ④该催化剂在该反应中可以重复使用


若实验③中观察到了明显的现象。通过以上实验,判断三种金属的活动性由弱到强的顺序为。实验①~④中,不需要做的实验是(填序号)。

①步骤②中发生了两个反应: 和。
②图中滤渣的成分是,写出加入稀盐酸发生反应的化学方程式。
③步骤①中参加反应的氯化铁与铜的质量比为。
![]()
其中步骤①发生反应的化学方程式。
①过滤;②加稍过量稀盐酸;③蒸发;④加稍过量Na2CO3溶液;⑤加稍过量BaCl2溶液

A.装置甲:制NH3B.装置乙:制NaHCO3
C.装置丙:分离NaHCO3D.装置丁:干燥Na2CO3




①若打开K1、关闭K2时,利用I、Ⅱ(里面装水)装置,实验室可以制取气体;
②利用Ⅰ、Ⅲ(里面装水)装置可以测定空气中氧气的含量。当关闭K、K1、K2 , 用凸透镜引燃B中的足量白磷,待冷却后打开K2 , 整个实验过程中的现象是。
③若B中盛放CO2 , A中盛放NaOH溶液,Ⅲ放稀盐酸,验证CO2能与NaOH发生反应,操作是。
【查阅资料】SO2能使品红溶液褪色;SO2易与KMnO4溶液反应而被吸收,并使其褪色;③SO2能使Ba(OH)2溶液和澄清石灰水变浑浊;④CO和CO2均不能使品红溶液褪色,也不与高锰酸钾溶液反应。以下实验中试剂瓶中的药品均足量。

【解释与结论】
若装置按C→D→A→B→E→F的顺序连接,则无法验证的气体是。
甲乙两同学在学习酸的化学性质时做了如图所示实验:

甲同学实验时没有观察到明显现象,乙同学实验时观察到有气泡发生:甲乙同学将反应完成后试管中的溶液倒入,洁净的废液杯中,没有观察到明显现象.
【提出问题】废液杯中溶液的溶质是什么?
猜想2:废液中含有的溶质为NaCl、CaCl2、HCl
猜想3:废液中含有的溶质为(写化学式)
【查阅资料】氢氧化铝能溶解在过量的氢氧化钠溶液中,生成偏铝酸钠(NaAlO2),有关化学反应方程式为:Al(OH)3+NaOH=NaAlO2+2H2O
