
选项 | A | B | C | D |
实验装置 |
|
|
|
|
实验现象或目的 | 分离I2和KMnO4固体 | 浓氨水与浓硫酸反应 | 制备Fe(OH)2 , 并观察其颜色 | 检验乙炔气体可使酸性高锰酸钾溶液褪色 |



回答下列问题:

已知:①有关金属离子形成氢氧化物沉淀的pH范围如下:
金属离子 | Fe2+ | Fe3+ | Co2+ |
开始沉淀的pH | 7.5 | 2.2 | 6.7 |
完全沉淀的pH | 9.5 | 3.0 | 8.7 |
②在pH为4~6时,Fe3+水解生成含Fe(OH)3·nFe3+·(n-x) 胶粒的胶体;
③金属钴与铁具有相似的化学性质;
④氧化性:Co3+>ClO-。
回答下列问题:

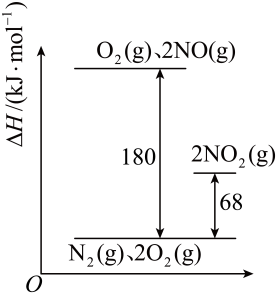
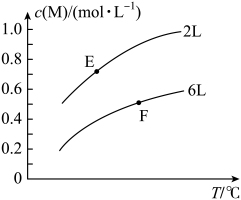
I.2NO(g)+O2(g)⇌2NO2(g) K1=3. 3×1013
II.2NO(g)⇌N2(g)+O2(g) K2=2. 2× 1030
则该温度下,反应III:2NO2(g)⇌N2(g)+2O2(g) K3= (计算结果保留一位小数),反应II与反应III相比分解趋势较大的反应是(填“反应II”或“反应III ”)。
序号 | c(NO)/(mol·L-1) | c(H2)/ (mol·L-1) | v正/(mol·L-1·min-1) |
I | 0.10 | 0.10 | 0.414k正 |
II | 0.10 | 0.20 | 0.828k正 |
III | 0.30 | 0.10 | 3.726k正 |
①v正 =k正cm(NO)·cn(H2)中,m=、n=。
②经研究,有人提出上述反应分两步进行: I. 2NO(g)+ H2 (g)=N2 (g) + H2O2(g);II. H2(g)+H2O2(g)=2H2O(g)。化学总反应由较慢的一步反应决定。上述反应中II反应较快,则反应I正反应活化能 (填“大于”“小于”或“等于”)反应II正反应活化能。

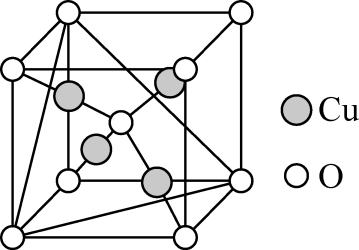
①苯环上有三个取代基,苯环上的一氯代物有两种;
②能发生水解反应,且水解产物之一能与FeCl3溶液发生显色反应;
③能发生银镜反应。
其中核磁共振氢谱有五组峰,峰面积之比为12:2:2: 1: 1的结构简式为、。