
 量取液体
B .
量取液体
B . 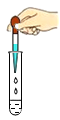 滴加液体
C .
滴加液体
C .  加热液体
D .
加热液体
D .  取用固体
取用固体
选项 | 物质 | 实验目的 | 主要实验操作 |
A | 合成纤维和羊毛线 | 鉴别 | 取样,灼烧,闻气味 |
B | Fe粉和CuSO4粉末 | 分离 | 溶解,过滤,洗涤,烘干,蒸发结晶 |
C | 碳酸钠与硫酸反应后,硫酸是否有剩余 | 检验 | 取样,滴加硝酸钡溶液,观察有无沉淀 |
D | 除去硝酸钠中混有的少量氯化钠 | 除杂 | 溶解、蒸发结晶、过滤 |
|
|
|
|
A.水通电,电解生成两种气体的体积变化 | B.加热两份等质量的氯酸钾固体制取氧气 | C.足量镁条在密闭容器中燃烧 | D.将铁钉加入足量的硫酸铜溶液中 |
①取试样溶于水,搅拌、过滤,得到无色澄清溶液A和白色沉淀B;
②取上述无色澄清溶液A,通入适量的CO2 , 生成白色沉淀C;
③取上述白色沉淀B,加入过量的稀硝酸,沉淀全部消失.
综合上述实验现象,下列判断正确的是( )
热情。

①航天员王亚平通过化学实验“变”出五色的奥运五环,这个化学实验用到的试剂有溶液、KI溶液、
溶液、
溶液,这四种溶液的溶质中,属于有机物的是(填字母序号)。
A.CH3COOH B.KI C.KIO3 D.
②在空间站中有电解水制氧系统,该系统利用循环水制取氧气,从而使氧气可重复供人呼吸,而生成的氢气可以与收集到的CO2在特殊反应器内转化为水和甲烷(CH4)。写出氢气与二氧化碳在催化剂作用下反应生成水和甲烷(CH4)的化学方程式:。


①在t1℃时,的溶解度为g。
②在t1℃时,向50g水中加入6g固体,经搅拌充分溶解,所得溶液的质量为。
③将t2℃时相同质量的饱和溶液和NaCl饱和溶液均降温至t1℃,此时所得两溶液的溶质质量分数相比较为(填“前者大”“后者大”或“相等”)。

写出该反应的化学方程式:;该反应属于(填基本反应类型),硅片太阳能电池将太阳能转化成电能,请说明太阳能电池的优点(写出一点即可)。


 表示的粒子在化学反应中易(填“得”或“失”)电子,形成的离子符号为。
表示的粒子在化学反应中易(填“得”或“失”)电子,形成的离子符号为。

已知:
①物质溶解性:难溶于水,
难溶于水;
② , Li与碱溶液不发生反应;
③ , 氯气是一种有毒的气体;
④部分金属离子形成氢氧化物沉淀的pH见下表。
金属离子 | Fe3+ | Co2+ | Co3+ | Al3+ |
pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
请回答:

①铜片 ②塑料 ③铁 ④石墨
《天工开物》中记载“石灰淹苗足”,利用了中和反应的原理,如果土壤呈酸性是因为有硝酸,写出氢氧化钙与其反应的化学方程式。下列应用原理与其不同的是(填字母序号)。
A.服用含Al(OH)3的药物治疗胃酸过多
B.用熟石灰处理硫酸厂的酸性废水
C.用稀盐酸除去钢铁表面的铁锈
D.用稀氨水处理蚊虫叮咬处(含蚁酸)
通过pH传感器和温度传感器完成以下实验:向40mL质量分数为0.4%的氢氧化钠溶液中逐滴滴入稀盐酸,测定溶液的pH随滴入稀盐酸体积的变化情况如图1所示。利用温度传感器测得反应过程中溶液温度随时间变化的曲线如图2所示。


如图1,向A点对应溶液中滴加无色酚酞溶液,溶液呈色。
有同学提出质疑,溶液温度升高,还可能是因为,请你设计实验证明中和反应是放热反应,实验方案是 。