|
废液来源 |
检测方法和结果 |
|
甲班 |
观察废液呈无色 |
|
乙班 |
观察废液呈红色 |

请你根据实验现象判断,对该废液的溶质的说法错误的是( )




猜想一:是小水滴。因为盐酸溶液中的水受热会汽化上升,在试管口液化成小水滴。
猜想二:是盐酸小液滴。因为浓盐酸具有性,可能实验中使用的盐酸浓度过高,试管口就会形 成盐酸小液滴。
同学们将干燥的蓝色石蕊试纸放在内有正在反应的镁条和盐酸的试管口,试纸,证明猜想二是 合理的。
Ⅱ. 小柯提出质疑:为什么刚才打开盛放实验所用盐酸的试剂瓶,瓶口没有白雾,却在反应过程中出现白 雾?
小柯联系反应时试管外壁很烫, 于是猜想:白雾的形成可能与温度有关。
他用试管取少量盐酸,将干燥的蓝色石蕊试纸放在试管口,试纸不变红;然后 (填操作), 将(选填“干燥的”、“湿润的”) 蓝色石蕊试纸放在试管口,试纸变红。
得出结论: 这种盐酸浓度并不高,是镁和盐酸反应放热促使盐酸形成白雾。
实验1:小乐在试管中放入一枚未打磨的铝片,然后注入适量pH=4的稀盐酸。铝片与稀盐酸反应产生氢气的速率随时间变化的图线如图甲所示。

实验2:小乐将另一枚打磨过的铝片与适量pH=4的稀硫酸反应,结果生成氢气速率很慢。
针对铝片与稀盐酸和稀硫酸反应速率不同的现象,小乐提出了如下猜想:
猜想1:盐酸中的氯离子对反应起促进作用;
猜想2:硫酸中的硫酸根离子对反应起阻碍作用。
为了验证猜想,小乐设计了如图乙所示实验。



①金属表面除锈 ②除去氯化钠中少量的氢氧化钠 ③实验室制二氧化碳
①铁 ②碳酸钠 ③氧化铁 ④氢氧化镁
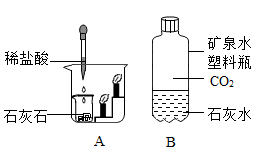
还可得出的化学性质.因此可利用二氧化碳来.

求:
| 加入稀盐酸的次序 | 1 | 2 | 3 | 4 |
| 加入稀盐酸的质量(克) | 10 | 10 | 10 | 10 |
| 剩余固体的质量(克) | 4.0 | m | 1.2 | 1.2 |