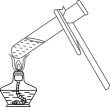
B . 滴加液体
B . 滴加液体 D . 验满
D . 验满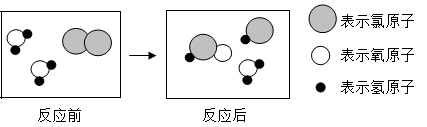
 在一定温度下,向不饱和的硝酸钾溶液中加入硝酸钾固体
B .
在一定温度下,向不饱和的硝酸钾溶液中加入硝酸钾固体
B .  向氢氧化钠溶液中加入一定量的水
C .
向氢氧化钠溶液中加入一定量的水
C . 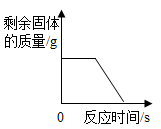 加热一定量氯酸钾和二氧化锰的混合物
D .
加热一定量氯酸钾和二氧化锰的混合物
D . 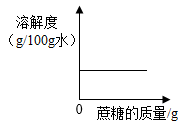 20℃时,向蔗糖的不饱和溶液中不断加入蔗糖固体
20℃时,向蔗糖的不饱和溶液中不断加入蔗糖固体
|
选项 |
物质 |
杂质 |
试剂与操作 |
|
A |
KNO3 |
NaCl |
加水溶解、蒸发结晶、过滤 |
|
B |
CO |
CO2 |
通过灼热的氧化铜 |
|
C |
Na2SO4溶液 |
MgSO4 |
加氢氧化钡溶液至不再产生沉淀,过滤 |
|
D |
NaCl |
Na2CO3 |
加入过量的稀盐酸至不再产生气泡,蒸发结晶 |
|
温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
|
|
溶解度/g |
KNO3 |
13.3 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
|
NaCl |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
|
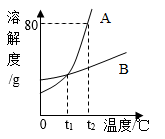
A.t1℃时,两种物质饱和溶液中溶质质量分数相同
B.t2℃时,等质量的两种物质的饱和溶液中所含溶剂的质量相同
C.t1℃大于20℃
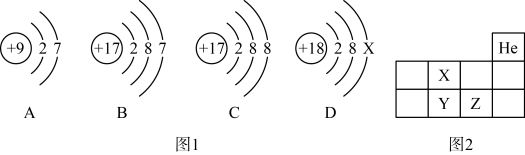
A.原子序数:Z>Y
B.核外电子数:X=Y
C.Y和Z处于同一周期
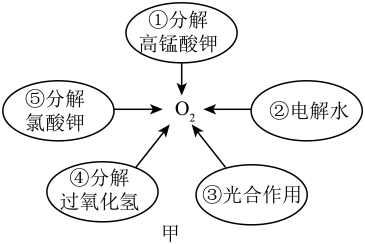
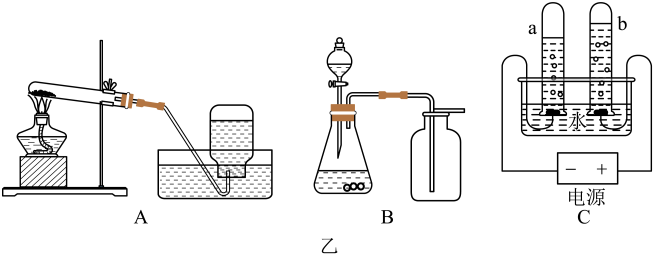
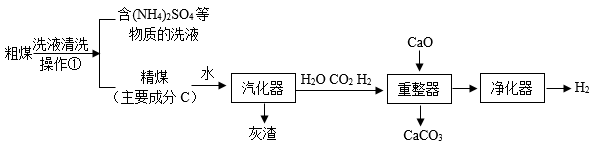
【提出问题】生锈铁钉与一定量稀硫酸反应后所得溶液中的溶质是什么?
【查阅资料】Fe3+与无色硫氰化钾溶液相遇出现血红色溶液。
实验步骤 | 实验现象 |
①取一枚生锈铁钉用蒸馏水洗净,再置于洁净试管中 | 铁钉表面有红褐色的铁锈 |
②向步骤①的试管内加入一定量稀硫酸 | 铁锈逐渐溶解,溶液由无色变为色,一会儿后产生气泡,最终溶液呈浅绿色 |
③当该试管内不再产生气泡时,取出铁钉,剩下溶液M,铁钉用蒸馏水洗净观察 | 铁钉表面呈银白色 |
写出步骤②中铁锈溶解的化学方程式。
【交流讨论】同学们对溶液M中没有溶质硫酸铁感到困惑,为此展开讨论。
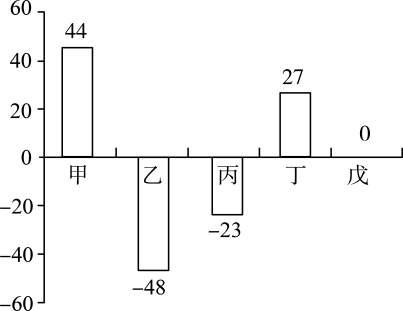
甲同学:反应过程中氢气与硫酸铁反应生成了硫酸亚铁。
乙同学:反应过程中铁与硫酸铁反应生成了硫酸亚铁。
请设计可证明某位同学观点成立的一组对比实验方案:。
若乙同学观点成立,则相应的化学方程式为。
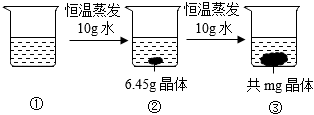
|
加稀盐酸的次数 |
第一次 |
第二次 |
|
加稀盐酸的质量/g |
25 |
25 |
|
生成二氧化碳的质量/g |
2.2 |
1.1 |