
 B . 倾倒液体
B . 倾倒液体 C . 过滤
C . 过滤 D . 干燥氧气
D . 干燥氧气

选项 | 实验目的 | 实验操作 |
A | 除去Fe中少量Fe2O3杂质 | 加入足量稀硫酸,过滤 |
B | 检验氢氧化钠是否变质 | 取样,向其中滴加少量稀盐酸 |
C | 检验某固体为碳酸盐 | 取样,滴加盐酸,将生成的气体通入澄清石灰水 |
D | 配制48g质量分数为6%的NaCl溶液 | 用托盘天平称量2.88gNaCl倒入烧杯中,用量筒量取所需水于烧杯中,用玻璃棒搅拌 |



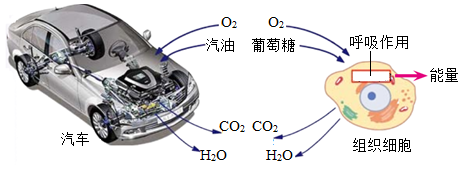
①第1步的化学方程式为,属于(填基本反应类型)。
②第2步合成乙酸的化学方程式为 , X的化学式为。
③3kg乙酸(CH3COOH)中,含有碳元素的质量为。
家庭中可用醋酸除水垢[主要成分为CaCO3和Mg(OH)2],请写出除水垢时发生的中和反应的化学方程式(提示:若金属元素H化合价为+1,醋酸盐书写形式为CH3COOM)。

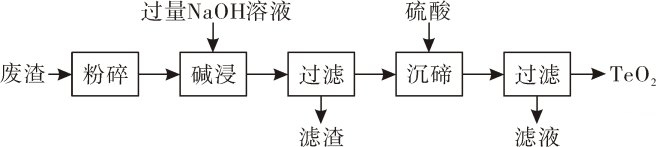
已知:TeO2微溶于水,能与NaOH溶液发生反应

①若用溶质质量分数为30%的H2O2溶液和MnO2制备氧气,反应速率太快。为获得平稳的气流,图1中最合适的是(填标号)。
②已知:用H2O2制取氧气时,也可用铂丝代替MnO2作催化剂。如图2中甲装置所示,若制备过程中体系内压强过大,则安全管中的现象是,此时应(填操作),使反应停止。
③用图2中乙装置进行铁丝在氧气里燃烧的实验,可观察到的现象是,实验时集气瓶炸裂,可能的原因是。

【实验一:探究锌、铁、银三种金属的活动性】
步骤①在试管中取少量盐酸,插入铁丝,充分作用;
步骤②在①所得的溶液中,插入银丝,充分作用;
步骤③在②所得的溶液中插入锌丝,充分作用。


