①C(s)+O2(g)=CO2(g) ∆H1 C(s)+O2(g)=CO (g) ∆H2
②S(s)+O2(g)=SO2(g) ∆H3 S(g)+O2(g)=SO2(g) ∆H4
③H2(g)+O2(g)=H2O(l) ∆H5 2H2(g)+O2(g)=2H2O(l) ∆H6
④CaO(s)+H2O(l)=Ca(OH)2(s) ∆H7 CaCO3(s)=CaO(s)+CO2(g) ∆H8
①2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH= -2600 KJ•mol-1
②2C6H6(g)+15O2(g)=12CO2(g)+6H2O(l) ΔH= -6590 KJ•mol-1
①CH3COOH(1)+2O2(g)=2CO2(g)+2H2O(l)△H1=-870.3kJ·mol-1
②C(s)+O2(g)=CO2(g)△H2=-393.5kJ·mol-1
③2H2(g)+O2(g)=2H2O(1)△H3=-571.6kJ·mol-1
写出由C(s)、H2(g)和O2(g)化合生成CH3COOH(l)的热化学方程式:。
①通过化学键的键能计算。已知:
化学键种类 | H-H | Cl-Cl | H-Cl |
键能(kJ/mol) | 436 | 247 | 434 |
计算可得:H2(g)+Cl2(g)=2HCl(g) △H= kJ·mol-1
②通过盖斯定律可计算。已知在25℃、101 kPa时:
I.2Na(s)+O2(g)=Na2O(s) △H=-414 kJ·mol-1
II.2Na(s)+O2(g)=Na2O2(s) △H=-511 kJ·mol-1
写出Na2O2与Na反应生成Na2O的热化学方程式:。
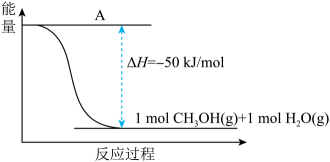
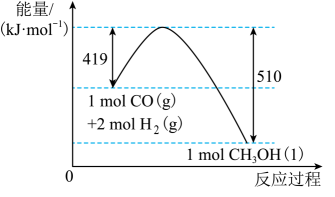
①补全上图:图中A处应填入。
②该反应需要加入铜-锌基催化剂。加入催化剂后,该反应的△H(填“变大”“变小”或“不变”)。
③某研究者分别以甲醇和汽油做燃料,实验测得在发动机高负荷工作情况下,汽车尾气中CO的百分含量与汽车的加速性能的关系如图所示。
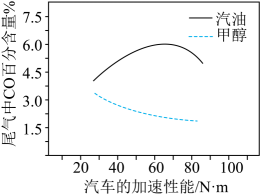
据图信息分析,与汽油相比,甲醇作为燃料的优点是。
①氧化钙与水反应;②石灰石在高温下的分解反应;③酸碱中和反应;④二氧化碳通过炽热的炭发生的反应;⑤食物因氧化而腐败发生的反应;⑥与
的反应;⑦干冰汽化。

RWGS反应:
反应ⅰ
副反应:
反应ⅱ
①已知:
则。
②混合动力汽车所用的燃料之一是乙醇,lg乙醇完全燃烧生成CO2气体和液态H2O放出30.0kJ热量,写出乙醇燃烧的燃烧热的热化学方程式。