| 分类 组合 | 酸性氧化物 | 酸 | 盐 | 混合物 | 电解质 |
| A | CaO | HClO | 烧碱 | 漂白粉 | H2O |
| B | CO | H2SO4 | NaOH | 碱石灰 | 蔗糖 |
| C | CO2 | Al(OH)3 | NaHCO3 | CuSO4·5H2O | NH3 |
| D | SO2 | HNO3 | CaCO3 | Fe(OH)3胶体 | KCl |


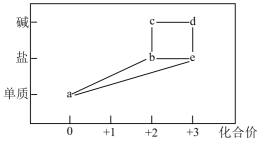

发生器中反应为
(未配平),下列关于
生产流程的相关说法不正确的是( )

|
|
|
|
将FeCl3饱和溶液滴入热NaOH溶液中制备氢氧化铁胶体 | 一段时间后,若往烧杯中液体滴加硝酸酸化硝酸银有白色沉淀,则半透膜破损 | 装置可用于固体碳酸氢铵加热分解 | 装置可用于比较碳酸钠和碳酸氢钠的热稳定性 |
A | B | C | D |
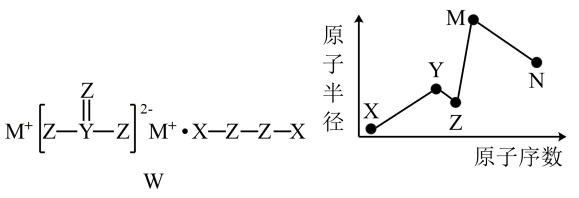

A.转移溶液前容量瓶中存在少量蒸馏水 B.所称取的晶体失去了部分结晶水
C.定容前未洗涤烧杯和玻璃棒 D.定容时仰视容量瓶刻度线

①为配制上述稀硫酸,除了容量瓶、烧杯、玻璃棒外,还缺少的玻璃仪器是、。
②在配制过程中,下列实验操作可能导致配制的硫酸溶液浓度偏低的是(填序号)。
A.定容时仰视刻度线
B.定容后经振荡、摇匀、静置后,发现液面下降,再加适量的蒸馏水
C.浓硫酸在烧杯中加水稀释后,未冷却就向容量瓶中转移
D.把洗涤量筒所产生的洗涤液注入容量瓶
3ClO- +2Fe3++10OH- = 2FeO42- +3Cl- +5H2O, 该反应中氧化剂是,氧化产物是。
②用单线桥法表示上述反应中电子转移的方向和数目:。

①A中反应的化学方程式为。
②E中收集的气体主要是 。