 点燃酒精灯
B .
点燃酒精灯
B .  倾倒液体
C .
倾倒液体
C .  读取液体的体积
D .
读取液体的体积
D .  取用固体
取用固体
选项 | 事实 | 认识 |
A | 水蒸发变成水蒸气 | 分子大小发生改变 |
B | 50L水和50L酒精混合后的体积小于100L | 分子之间有间隔 |
C | 一滴水中含有约1.67×1021个水分子 | 水分子的体积和质量都很小 |
D | N2的化学性质不活泼,O2的化学性质比较活泼 | 不同分子性质不同 |
 B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 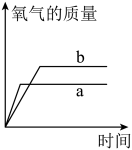
气体 | X | Y | 二氧化碳 | 水 | 其他气体 |
吸入气体 | 78% | 21% | 0.03% | 0.02% | 0.95% |
呼出气体 | 75% | 15% | 3.68% | 5.44% | 0.88% |
①请你判断:表中Y是。
②将澄清石灰水倒入装有呼出气体的集气瓶中,振荡,发现,说明呼出气体中的二氧化碳含量比空气中的要高。
③X气体在呼吸过程中没有参与化学反应,但在呼出的气体中体积分数却减少了,其原因是。


反应①,属于反应。
反应③,属于反应。
I.制硫酸:


“原料气”中的制备:工业上要制得大量的N2 , 通常可采用分离的方法得到,其原理是利用氧气和氮气的不同,该过程属于(选填“物理”、“化学”)变化。
Ⅲ.制备硫酸铵:
将NH3通入稀释后的硫酸溶液中,得到硫酸铵。

1.在试管中加入2m15%的过氧化氢溶液,将带火星的木条伸入试管中,观察现象 | 1.带火星的木条没有明显变化 |
2.取1gCuO粉末放在放在步骤1中的试管中,将,观察现象 | 2. |
结论:氧化铜能加快过氧化氢的分解速率。
实验目的:探究氧化铜的化学性质在化学反应前后是否发生改变。
实验步骤 | 实验现象 |
待实验一第2步的试管中没有气泡时,重新加入2mL过氧化氢溶液,并将带火星的木条伸入试管中,观察现象 |
结论:氧化铜的化学性质在化学反应前后没有发生改变。
小芳同学根据以上的实验现象,得出氧化铜是过氧化氢溶液分解的催化剂。请写出在该实验中过氧化氢溶液分解反应的符号表达式。
经过讨论,小明同学认为仅凭实验一和实验二,不能证明氧化铜是过氧化氢分解的催化剂。小明同学补充的实验是:待反应结束后,将试管里的物质进行过滤、洗涤、干燥,再次(填操作名称),其目的是。最终大家一起完成了对这个猜想的验证。
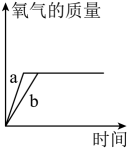
在这个化学反应中,下列说法正确的是(填编号)。
①不加二氧化锰就不会放出氧气
②不加二氧化锰放出氧气速率慢
③加入二氧化锰后生成的氧气总质量会增加
④加入二氧化锰后生成的氧气总质量不变