选项 | 实验目的 | 实验设计 | 选项 | 实验目的 | 实验设计 |
A | 探究CO2与水发生反应 |
| B | 探究温度对分子运动快慢的影响 |
|
C | 验证质量守恒定律 |
| D | 除去CO2中少量的CO |
|
选项 | 物质 | 所含杂质 | 除杂质的方法 |
A | Cu | Fe | 加入足量的稀硫酸,过滤,洗涤,干燥 |
B | N2 | O2 | 将混合气体通过灼热的铜网 |
C | CO2 | CO | 将混合气体点燃 |
D | Cu(NO3)2溶液 | AgNO3 | 加入过量的铜粉,过滤 |
选项 | 实验目的 | 所用试剂或方法 |
A | 除去氧化铜中的碳粉 | 高温加热 |
B | 鉴别氧化铜和碳粉 | 观察颜色 |
C | 除去CO2中的CO | 点燃 |
D | 鉴别CO和CO2 | 分别通入紫色石蕊溶液 |
序号 | 化学反应事实 | 影响反应的因素 |
A | 铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧 | 反应物浓度 |
B | 碳常温下不与氧气发生反应,而在点燃时能与氧气反应 | 反应温度 |
C | 双氧水在常温下较难分解,而加入二氧化锰后迅速分解 | 催化剂 |
D | 铜片在空气中很难燃烧,铜粉在空气中较易燃烧 | 反应物的种类 |




已知:钡元素化合物的化学性质与钙元素化合物的化学性质相似。下表是不同温度下Ca(OH)2和Ba(OH)2的溶解度。
温度(℃) | 0 | 20 | 25 | 60 | |
溶解度/g | Ba(OH)2 | 1.67 | 3.89 | 5.60 | 20.94 |
Ca(OH)2 | 0.189 | 0.173 | 0.148 | 0.121 | |


①所选装置的连接顺序为(从左到右填写装置序号字母)。
②上述方法制氧气的化学方程式为。
③若把G装置中的浓硫酸换成水并盛满,用来收集难溶于水的气体时,气体从(填“a”或“b”)端通入。
实验操作 | 实验现象 | 实验结论 | |
① | 分别用A、B、C三支试管取三种溶液各少量,然后再各加入一定量的碳酸钠溶液 | A中 B中 C中无明显现象 | A中的原溶液是氯化钡溶液 B中的原溶液是稀硫酸 C中的原溶液是氢氧化钠溶液 |
上述实验结束后,该组同学将A、B、C三支试管中的废液倒入同一烧杯中,然后过滤得到滤液①.为确定滤液①的成分,同学们进一步做了如下实验探究:
实验操作 | 实验现象 | 实验分析 | |
② | 取少量滤液①于试管中,向其中加入足量的氯化钡溶液;过滤,得沉淀和滤液②,向沉淀中加入足量稀硝酸 | 产生白色沉淀 白色沉淀部分消失 | 根据实验现象可知,滤液①中含有 (填写溶质的化学式) |
③ | 取少量滤液②于试管中, | 根据实验现象可知,滤液②中含有氢氧化钠 |
【选择试剂】同学们经过讨论,选择的试剂有:①氢氧化钠溶液②碳酸钠溶液③氯化钡溶液。
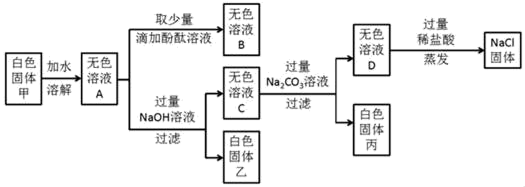
【探究过程】取步骤Ⅰ后的粗盐溶液进行下列实验

滴加甲、乙、丙三种试剂的正确顺序最多有种,下列顺序合理的是(填字母)。
A.①②③ B.③②① C.①③②
靖博同学认为,上述实验可以将甲、 乙、丙三种溶液改成两种溶液,分别为(按加入的先后顺序填写溶质的化学式)。
【查阅资料】①浓硫酸是一种常见的干燥剂;水能使白色无水硫酸铜固体变蓝色。
②鸡蛋壳的主要成分是CaCO3 , 杂质不与醋酸反应,白醋由醋酸(化学式为CH3COOH)和水组成。
③加热的条件下氢气、一氧化碳都能使氧化铜转化为铜。

【实验预测】
若气体中含有氧气则F中的实验现象为;若气体中含有氢气但不含有一氧化碳,则G中的实验现象应为,H中的现象应为。
【进行实验】实验中只观察到D处澄清石灰水变浑浊其余都无明显现象。
CaCO3与CH3COOH反应会产生。通过询问老师获知,生成物中有一种物质叫醋酸钙[Ca(CH3COO)2]。
将20.0g的鸡蛋壳与足量的稀醋酸按上图进行实验,D装置增重了5.5g,则生成二氧化碳的质量为g;
设解:设20.0g的鸡蛋壳中的碳酸钙的质量为x。
写出方程式
写出相对分子质量、已知量、未知量
列比例式
求解x=12.5g
该鸡蛋壳中碳酸钙的质量分数为(列式并计算结果)