

选项 | 实验目的 | 实验方法 |
A | 检验甲烷中含有氢元素 | 点燃后在火焰上方罩干冷小烧杯 |
B | 分离硝酸钾和氯化钠的固体混合物 | 加水溶解后,蒸发溶剂 |
C | 鉴别稀硫酸和稀盐酸 | 加入 |
D | 除去 | 将气体通过加热的 |

①石墨烯海水淡化膜允许(填微粒符号)通过。
②石墨烯、金刚石和都属于碳单质,下列说法中正确的是(选填字母)。
A.都由碳元素组成 B.都由碳原子构成 C.物理性质相似

①试管(选填“a”或“b”)中产生的气体可使带火星的木条复燃。
②写出电解水的化学反应方程式。
③气态储氢是将氢气压缩存储于高压罐中,请从微观角度分析氢气能被压缩的原因。
④氢燃料电池汽车基本实现碳的“零排放”。目前在生活生产中大量使用氢能源还存在一定困难,原因是(选填字母)。
A.氢气本身无毒 B.氢气制取成本高和贮存困难
C.氢气燃烧放出热量多 D.氢气燃烧产物不污染空气

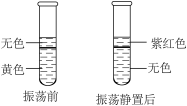
①甲同学设计如图3所示实验:将无色酚酞溶液滴入试管中,溶液颜色变为红色;再将浓盐酸滴入试管b中,一段时间后,a中溶液红色消失,说明与
发生了反应。该反应的基本类型是。该实验还说明浓盐酸的性质有酸性和。
②乙同学将氢氧化钙溶液与稀盐酸混合,然后检验了混合液中含有和
, 他据此认为
与
发生了反应,且生成了
。你认为乙同学是否找到了反应发生的证据?请说出你的观点并阐述理由:。



①实验1:实验中,观察到发出白光后铁丝并未燃烧,原因是。
②实验2:向两个盛有同样大小的铁片和铝片的试管中,分别滴加相同浓度的稀盐酸比较铁和铝的金属活动性强弱。实验之前铝片需要先用砂纸打磨的目的是。
③实验3:该反应的化学方程式为。
④在实验3的基础上,再补充一个实验可得出三种金属活动性顺序。将实验步骤和实验现象填入表中、
实验步骤(可用图示) | 实验现象 | 实验结论 |
【实验过程】学生利用如图所示装置,以收集的气体为标准,比较反应的快慢,实验方案如下表所示(分液漏斗可控制液体的滴加速度):

序号 | 温度 |
|
|
| 时间 |
1 | 20 | 5 | 40 | 37 | |
2 | 20 | 10 | 40 | 14 | |
3 | 20 | 5 | 40 | 氧化铜 | b |
4 | 80 | 5 | 40 | 29 |
【实验分析】
①写出实验3发生反应的化学方程式。
②对比实验1和2,得出的结论是。
③通过对比实验1和3,得出二氧化锰的催化效果比氧化铜强的实验依据是。
④实验中,使用注射器的优点是。
探究氯化物对溶液分解的影响。
氯化物 | |||
放出氧气的体积 | 2.0 | 4.0 | 420.0 |
| 0.30 | 0.60 | 63.18 |
【实验过程】反应条件:溶液,
氯化物,室温;实验时间:
。
【实验分析】
由上表数据可知溶液保存时应绝对避免引入的离子是(写离子符号)。
探究对
溶液分解的影响。
【实验过程】反应条件:溶液,
;用
溶液调
;实验时间:
。
【实验分析】
由图可知,为(填数字)时,
溶液的分解率最高。

“钙多宝”主要成分是 , 常温下能与水反应生成氢氧化钙和氧气。长时间存放的过氧化钙中含有的主要杂质是(填化学式)、
。