图像 |
|
|
|
|
设计实验 | 甲:向未经打磨的铝片中滴加适量稀盐酸 | 乙:向 | 丙:分别向等质量的 | 丁:足量红磷在密闭的集气瓶中燃烧 |
 B .
B .  C .
C .  D .
D . 

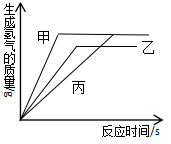
①Na、Mg、Zn三种金属都能置换出酸中的氢
②生成相同质量的氢气消耗金属的质量为Na>Mg=Zn
③生成相同质量的氢气消耗Na、Mg、Zn三种金属的质量比为23∶24∶65
④生成相同质量的氢气消耗Na、Mg、Zn三种金属的原子个数比为2∶1∶1



|
合金 |
合金的主要性能 |
主要成分及纯金属的性能 |
|
焊锡 |
熔点183 ℃ |
锡:熔点232℃;铅:熔点327 ℃ |
|
硬铝 |
强度和硬度好 |
铝、铜、镁等。硬度小,质软 |
|
不锈钢 |
抗腐蚀性好 |
铁、铬、镍等。纯铁抗腐蚀性能不如不锈钢 |
由表中信息可以推断,与组成合金的纯金属相比,合金的优点一般有(填序号,可多选)。
①强度更低
②硬度更高
③熔点更高
④抗腐蚀性更好

【查阅资料】
资料一:火柴头中含有氯酸钾、硫磺、二氧化锰,以及石蜡、炭粉等成分;一般红色火柴头所用的着色剂为氧化铁。
资料二:氧化铁不具有磁性,不能被磁化;四氧化三铁是具有磁性的黑色固体,故又称为磁性氧化铁
【建立假设】
假设一:燃烧后的火柴头成分中含有四氧化三铁。
假设二:燃烧后的火柴头成分中含有单质铁。
假设三:燃烧后的火柴头成分中含有四氧化三铁和单质铁。
步骤①:将燃烧后的火柴头研磨成粉末并装入试管;
步骤②:在试管中加入足量CuSO4溶液,充分反应。
步骤③:过滤并将得到的固体充分干燥,再用磁铁吸引。
【得出结论】
若假设三成立,则作为证据的实验现象应为。
尝试用科学原理解释火柴头中加入氯酸钾的目的。

【查阅资料】钠常温下就能与水发生剧烈反应,反应的化学方程式为2Na+2H2O=2NaOH+H2↑。
【提出猜想】猜想一:金属钠和硫酸铜溶液反应会有铜生成。
猜想二:金属钠和硫酸铜溶液反应,生成的沉淀只有氢氧化铜。
【实验及现象】切取不同大小的钠块分别投入到两种不同浓度的硫酸铜溶液中,有关产生沉淀的现象如表中所示。
|
实验编号 |
钠块大小 |
硫酸铜溶液 |
实验中产生沉淀的现象 |
|
① |
绿豆大小 |
稀溶液10mL |
产生蓝绿色沉淀 |
|
② |
绿豆大小 |
浓溶液10mL |
产生蓝色絮状沉淀 |
|
③ |
豌豆大小 |
稀溶液10mL |
产生蓝色絮状沉淀 |
|
④ |
豌豆大小 |
浓溶液10mL |
产生蓝色絮状沉淀,并出现黑色固体 |
小科咨询老师后得知蓝绿色沉淀为碱式铜盐。
【实验结论】
【实验反思】实验中生成氢氧化铜沉淀的原理是(用化学方程式表示)。