



物质 | 甲 | 乙 | 丙 | 丁 |
|
微观示意图 |
|
|
|
| |
反应前质量/g | 32 | 200 | 10 | 0 | |
反应后质量/g | 0 | x | y | z |



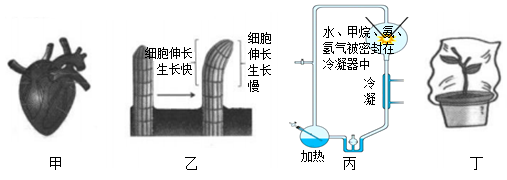
A.吸烟 B.紧张 C.肥胖 D.经常运动




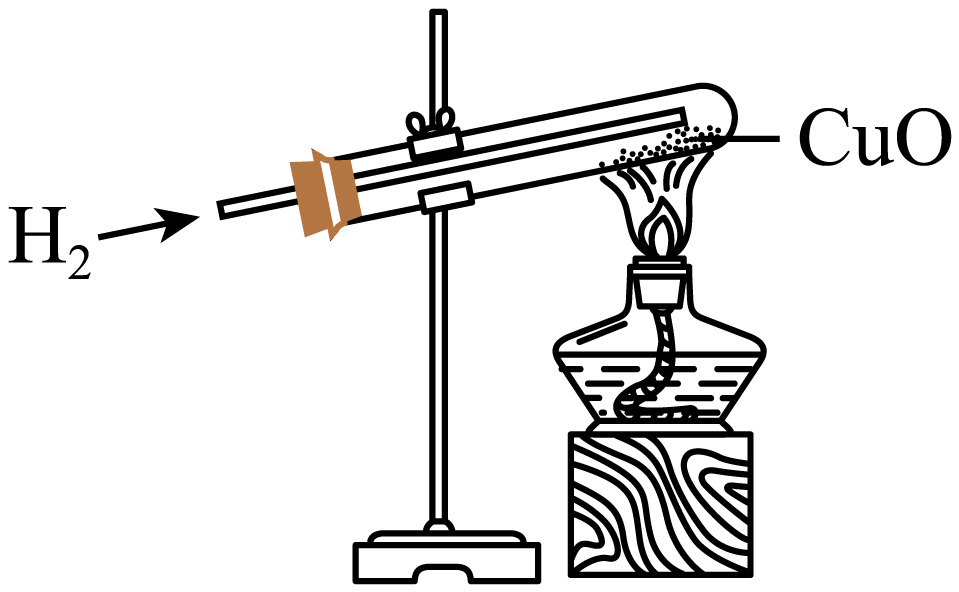
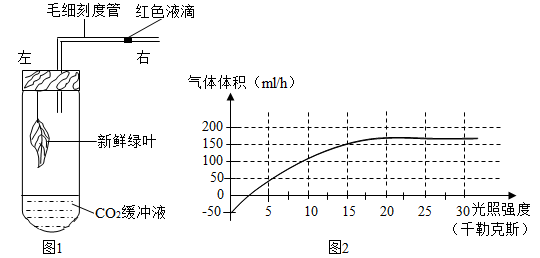
|
温度(℃) |
5 |
10 |
15 |
20 |
25 |
30 |
35 |
|
光照下吸收的二氧化碳量(mg/h) |
1.0 |
1.75 |
2.5 |
3.25 |
3.75 |
3.5 |
3.5 |
|
黑暗中释放的二氧化碳量(mg/h) |
0.5 |
0.75 |
1.0 |
1.5 |
2.25 |
3.0 |
3.5 |
①若实验过程中昼夜一直不停光照,则温度约为时植物生长速度最快。
②若每天提供12小时光照,其余时间黑暗处理;则24小时内植物有机物积累量最大时的温度约为。

⑴电流表量程应选。(填序号)
A. B.
C.
D.
⑵滑动变阻器规格应选。(填序号)
A. B.
C.
D.
⑶正确连接了实物电路,将L1接入电路。
⑷闭合开关S,调节滑动变阻器滑片,让电压表示数分别为 , 读出电流表示数,填在表中。根据表中数据,L1的额定功率
W。
实验次数 | 1 | 2 | 3 | 4 | 5 | |
电压 | 1.0 | 2.2 | 2.5 | 2.8 | 3.0 | |
电流 | 接入L1 | 0.10 | 0.22 | 0.25 | 0.28 | 0.30 |
接入L2 | 0.10 | 0.23 | 0.26 | 0.29 | 0.31 | |
⑸断开开关S,用L2替换L1 , 重复第(4)步测量操作,将测得的数据填入上表。
⑹该同学根据表中数据,计算L2的额定功率 , 他立即意识到这个结果不是L2的额定功率。要测得L2的额定功率,还需要的测量操作是:。
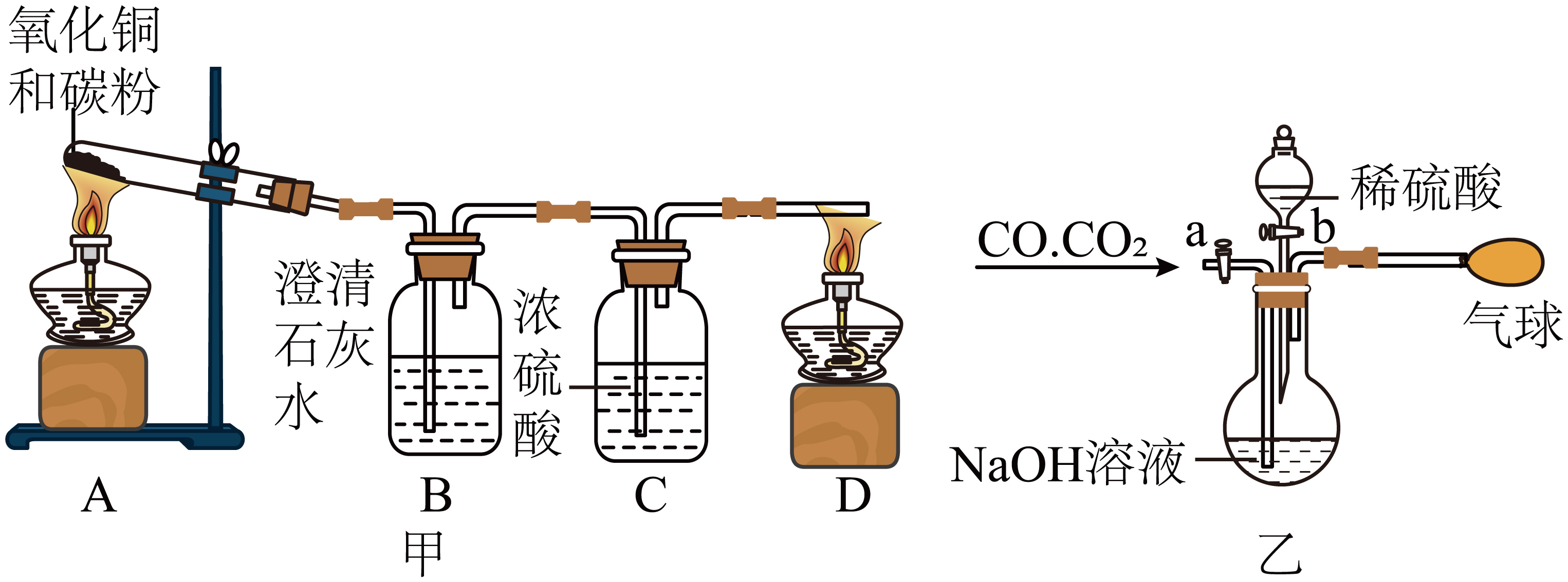
【提出问题】碳和氧化铜反应生成的气体是什么?
【作出猜想】猜想①:生成的气体可能是CO;
猜想②:生成的气体可能是CO2;
猜想③:生成的气体可能是CO和CO2.
【收集证据】
若观察到(填写现象),则说明生成气体中没有。
用电子天平测定表格中的四个数据:
反应前的质量 | 反应后的质量 | |
A(试管+固体) | m1 | m2 |
B+C(广口瓶+溶液) | m3 | m4 |
若猜想③成立,则存在的质量关系是(用m1.m2 , m3、m4来表示)
若反应生成物有一氧化碳和二氧化碳,他又设计了如图乙所示的装置分离CO和CO2(铁架台、铁夹等固定用装置已略去,a、b为活塞)。若想实现分离,活塞a和b应该如何操作?。
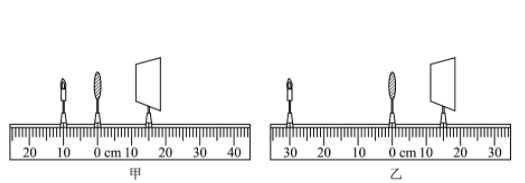
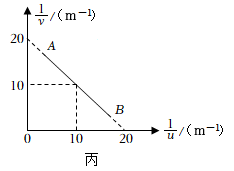
①若仅将凸透镜换成焦距相同直径较小的凸透镜,再次实验,光屏上所成的像与原来相比(选填“变小”“变暗”或“变不完整”)了;
②若将凸透镜换成直径大小相同、焦距稍小的凸透镜,再次实验,则需将屏(选填“向左”或“向右”)移动才能成清晰的像;


【查阅资料】①KOH与NaOH的化学性质相似。
请用化学方程式解释KOH变质的原因是(用化学方程式表示)。
②K2CO3溶液呈碱性,CaCl2溶液,KCl溶液呈中性。
【猜想假设】假设Ⅰ:只含KOH;假设Ⅱ:含KOH和K2CO3;假设Ⅲ:只含K2CO3.
【进行实验】
实验操作步骤 | 实验现象 | 实验结论 |
a、取少量样品于试管中,加入足量的稀盐酸 | 有气泡产生 | 假设错误 |
b、另取少量样品于试管中,加水溶解,加入过量的CaCl2溶液,振荡,静置 | 产生白色沉淀 | 猜想Ⅱ正确 |
c、取②中上层清液,滴加无色的酚酞试液 |
【拓展应用】完全变质的KOH也有利用价值,从K2CO3的组成或性质看,K2CO3在农业上的可以作为钾肥使用。




热敏电阻 | |||||||||||||||
温度/45℃ | 20 | 25 | 30 | 35 | 39 | 40 | 41 | 42 | 43 | 44 | 45 | 50 | 55 | 60 | 65 |
阻值/欧 | 600 | 480 | 390 | 300 | 240 | 230 | 220 | 210 | 200 | 190 | 180 | 150 | 120 | 100 | 85 |

①1000牛压力以下,坐垫最高温度不超过45℃;
②人离开后,坐垫始终低功率工作。
现有三种力敏电阻 , 其阻值随压力变化如图乙所示。写出你选择的力敏电阻以及在控制电路中的连接方式,并写出500牛压力下坐垫的最高温度值:。(线圈阻值忽略不计)

①往菜地的土壤中掺入一定比例沙子。
②将家禽、家畜的粪便及杂草等堆积一段时间“发酵”成肥料。
③搭配种植高矮不同的多品种蔬菜。
④夏天避免中午浇水,冬季避免傍晚浇水。
结合上述信息,综合运用所学知识,对以上经验作出解释。
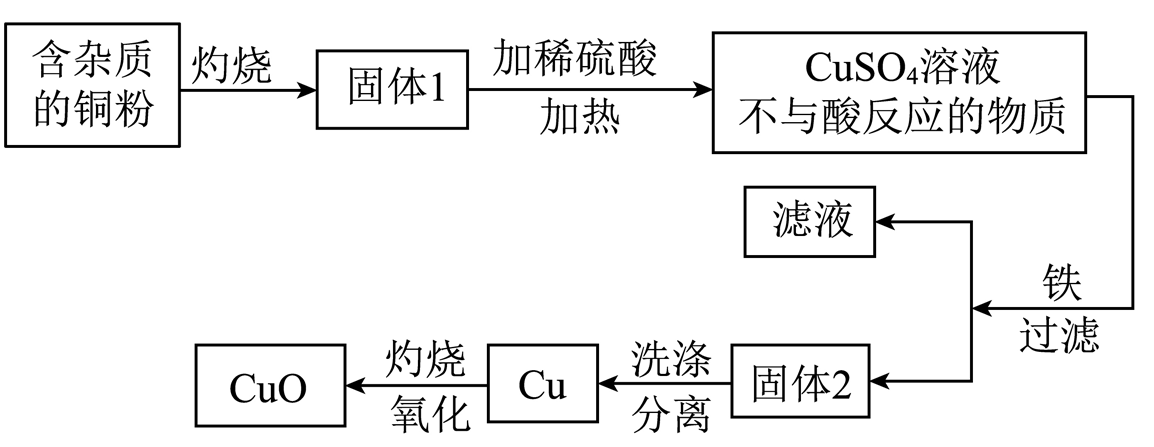
①固体1中加入稀硫酸,若溶液呈蓝色,说明该固体中一定有氧化铜
②固体1中加入稀硫酸,若有红色沉淀物,说明该固体中一定有氧化亚铜

①分离出的浓盐水是(选填“纯净物”或“混合物”)。
②某工厂淡化海水后得到的浓盐水和淡水中盐类物质含量如表(微量盐类忽略不计)。国家规定居民生活用水中盐类物质总含量≤500毫克·升-1 , 计算并推断所得淡水中盐类总含量(选填“达到”或“未达到”)生活用水的标准;该工厂一套淡化装置每小时产生浓盐水300升,其中含有NaCl千克。
盐类(含量/g·L-1) 水样 | 氯化钠 | 氯化镁 | 硫酸镁 | 硫酸钙 |
淡水 | 0.17 | 0.012 | 4.8×10-1 | 8.5×10-1 |
浓盐水 | 45.0 | 3.6 | 3.3 | 0.14 |

①加适量盐酸的目的是。
②用pH试纸检验溶液丙是否呈中性的操作是。
①海洋潮汐发电是利用了海水的能。
②小敏家两次电能表显示如图,他家这30天的用电量为千瓦时。某潮汐发电站发电机日平均发电量44万千瓦时,它最多可供万户类似小敏家庭的日用电。(结果保留整数)
