选项 | 现象或事实 | 解释 |
A | 用热的烧碱溶液洗去镀件油污 | Na2CO3可直接和油污反应 |
B | 漂白粉在空气中久置变质 | 漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
C | 施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用 | K2CO3与NH4Cl溶液反应生成氨气会降低氨肥肥效 |
D | FeCl3溶液可用于铜质印刷线路板制作 | FeCl3能从含有Cu2+的溶液中置换出铜 |




C(s)+O2(g)=CO2(g)△H=﹣393.5kJ•mol﹣1
则2Fe(s)+O2(g)═Fe2O3(s)的△H是( )

2A(g)+B(g)⇌3C(g)+4D(s),若经 2s后测得 C 的浓度为 0.9mol•L﹣1 , 现有下列几种说法:
①用物质 A 表示的反应的平均速率为 0.3mol•L﹣1•s﹣1
②用物质 D 表示的反应的平均速率为 0.6mol•L﹣1•s﹣1
③2s 时物质 A 的转化率为30%
④用A、B、C来表示反应速率,其速率之比=2:1:3
其中正确的是( )


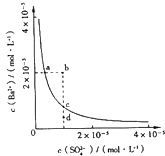
提示BaSO4(s)⇌Ba2+(aq)+SO42﹣(aq)的平衡常数Ksp=[Ba2+]•[SO42﹣],称为溶度积常数.
实验编号 | 起始浓度/(mol•L﹣1) | 反应后溶液的pH | |
c(HA) | c(KOH) | ||
① | 0.1 | 0.1 | 9 |
② | x | 0.2 | 7 |
下列判断不正确的是( )

空瓷舟质量m0/g | 瓷舟与钙的质量m1/g | 瓷舟与产物的质量m2/g |
14.80 | 15.08 | 15.15 |
①计算得到实验式CaxN2 , 其中x=.
②若通入的N2中混有少量O2 , 请比较x与3的大小,并给出判断依据:.

在一定质量范围内,加入不同质量的MnO2 , 测量所得气体体积,数据如下:
MnO2的质量/g | 0.1 | 0.2 | 0.4 |
40s末O2体积/mL | 49 | 61 | 86 |
由此得出的结论是,原因是.
试管 | Ⅰ | Ⅱ | Ⅲ |
滴加试剂 | 5滴0.1mol•L﹣1FeCl3 | 5滴0.1mol•L﹣1 CuCl2 | 5滴0.3mol•L﹣1 NaCl |
产生气泡情况 | 较快产生细小气泡 | 缓慢产生细小气泡 | 无气泡产生 |
结论是,实验Ⅲ的目的是.
氧化还原反应的化学方程式分别是和(按反应发生的顺序写).
②在上述实验过程中,分别检测出溶液中有二价锰、二价铁和一价铜,由此得出选择作为H2O2分解反应的催化剂需要满足的条件是.

①写出由纯SiHCl3制备高纯硅的化学反应方程式
②整个制备过程必须严格控制无水无氧.SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出配平的化学反应方程式,H2还原SiHCl3过程中若混入O2 , 可能引起的后果是.
①2O2(g)+N2(g)=N2O4 , (l)△H1
②N2(g)+2H2(g)=N2H4(l)△H2
③O2(g)+2H2(g)=2H2O(g)△H3
④2N2 H4 (1)+N2O4 (1)=3N2 (g)+4H2O(g)△H4=﹣1048.9kJ/mol
上述反应热效应之间的关系式为△H4=,联氨和N2O4可作为火箭助推剂,折算在标准状况下的数据,燃爆后气体的体积与燃爆前的体积之比为:
N2H4 | N2O4 | |
密度/g/cm3 | 1.004 | 1.44 |