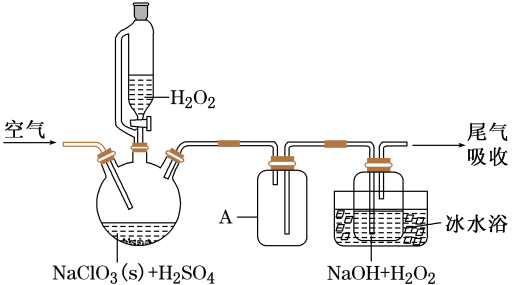
已知:2NaClO3+H2O2+H2SO4=2ClO2 ↑+O2↑+Na2SO4+2H2O
2ClO2+H2O2+2NaOH=2NaClO2+O2↑+2H2O
ClO2熔点-59℃、沸点11℃; H2O2沸点150℃
请回答:
①(用离子方程式表示);
②H2O2+Cl2= 2Cl-+O2+2H+。
I.在锥形瓶中加入足量的碘化钾,用50mL蒸馏水溶解后,再加入3mL稀硫酸;
Ⅱ.再向该锥形瓶中加入20.00 mL自来水;
Ⅲ.用0.0001 mol ·L-1 Na2S2O3溶液滴定测定锥形瓶中生成I2的量。(已知:I2+2=2I-+
),共用去20.00 mL Na2S2O3溶液。
计算可得自来水水样中ClO2的含量为mg/L(精确到0.01)。
微信扫码预览、分享更方便