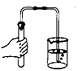
 检查装置气密性
B .
检查装置气密性
B .  熄灭酒精灯
C .
熄灭酒精灯
C . 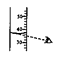 量取液体
D .
量取液体
D . 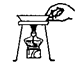 移走蒸发皿
移走蒸发皿
 稀释NaOH溶液
B .
稀释NaOH溶液
B .  镁带在足量氧气中燃烧
C .
镁带在足量氧气中燃烧
C .  饱和石灰水中加入氧化钙
D .
饱和石灰水中加入氧化钙
D .  氧气的溶解度
氧气的溶解度
 B .
B .  C .
C .  D .
D . 
实验一  实验二
实验二 
实验三 
①由实验一可知,CO2具有的物理性质是。
②在实验二中,发现B中铁丝不燃烧,其原因是,A中铁丝燃烧的化学方程式是。
③实验三为电解水装置通电一段时间后,试管a、b中产生气体的体积比约为,该实验证明水是由组成的化合物。
④食用油脂中含有亚油酸(C18H32O2),缺乏亚油酸会使人体发育不良。亚油酸中碳元素存在形态为(填“游离态”或“化合态”);氢元素与氧元素的质量比为;1molC18H32O2中约含个氧原子(用科学记数法表示)。
⑥人类社会的发展离不开能源,当今社会,人类利用的能源主要来自化石燃料化石燃料主要有煤、石油和。
⑦宏观辨识与微观探析是化学核心素养之一。如图是某反应的微观示意图。

Ⅰ.生成物中由原子直接构成的物质是(填“乙”或“丙”)。
Ⅱ.该变化的化学方程式为;反应类型属于(填“分解”或“化合”)反应。

①50℃时,硝酸钾的溶解度是;硝酸钾的溶解度随温度的升高而(填“增大”或“减小”)。
②硝酸钾和氯化钠都属于物质(填“难溶”、“微溶”、“可溶”或“易溶”)。
③“海水晒盐”利用的方法是(填“蒸发结晶”或“降温结晶”)。
④20℃时,如要提纯9g粗盐(粗盐中氯化钠含量约为80%),溶解时应选择(填“10mL”、“25mL”或“100mL”)规格的量筒量取所需要的水最为合适,理由是:。
⑤在20℃时,将等质量的硝酸钾和氯化钠分别加入到各盛有100g水的甲、乙两个烧杯中,充分搅拌后现象如图2所示,说法错误的是(填序号)。
A.烧杯乙中的上层溶液是饱和溶液
B.烧杯甲中溶液的溶质是硝酸钾
C.烧杯甲中溶液质量比烧杯乙中溶液质量大
D.将温度升高到50℃,烧杯乙中的固体不一定全部溶解

①写出仪器m和装置C的名称:仪器m,装置C。
②实验室用氯酸钾和二氧化锰制取氧气,反应的化学方程式是;选择E装置收集氧气,当看到,说明气体收集满了。
③实验室用大理石和稀盐酸制取二氧化碳,可选用的发生装置是(填字母序号);选择D装置收集时,检验CO2已满的方法是。
④实验室也可用过氧化氢溶液和二氧化锰制取氧气,为测定过氧化氢溶液的溶质质量分数,某学生将适量二氧化锰放入20g过氧化氢溶液,完全反应后,共收集到氧气0.025mol。
Ⅰ.求参加反应的过氧化氢的物质的量。(根据化学方程式列式计算)。
Ⅱ.该过氧化氢溶液中溶质的质量分数是。

I.“步骤d”过滤时用到玻璃棒,其作用为。
Ⅱ.小组同学通过上述实验得出结论:CuO可作过氧化氢分解的催化剂,支持该结论的实验证据有(填序号)。
A.“步骤a”带火星的木条不复燃
B.“步骤c”带火星的木条复燃
C.“步骤f”固体质量为0.2g
D.“步骤g”溶液中有气泡放出,带火星的木条复燃

Ⅰ.探究CO与CuO的反应:通入气体一氧化碳,M处为氧化铜,加热前先通一氧化碳的目的是;M处反应的化学方程式为;澄清石灰水的作用是。
Ⅱ.探究CO2与C的反应(改为酒精喷灯):通入气体二氧化碳,M处为木炭,观察到玻璃管中的现象是,M处反应的化学方程式为。导管a处点燃的目的是。
(提出问题)剩余固体成分是什么?
(猜想与假设)
猜想一:。
猜想二:是氧化钙与碳酸钙的混合物。
(实验探究)
|
实验步骤 |
实验现象 |
|
|
步骤1 |
取一定量的剩余固体于试管中,加入一定量的水,振荡、静置。取上层清液,滴加无色酚酞试液。 |
|
|
步骤2 |
另取一定量的剩余固体于试管中,加入足量。 |
有气泡产生 |
(探究结论)通过探究,猜想二成立。