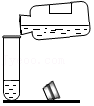
B .
B . 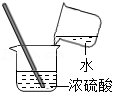
C .
C . 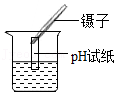
D .
D . 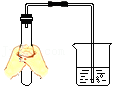
| 选项 | 实验目的 | 实验方案 |
| A | 除去稀硫酸中的FeSO4 | 加入适量锌粉 |
| B | 除去CO2中的CO | 将气体通入NaOH溶液 |
| C | 除去CaCl2溶液中的HCl | 加过量CaCO3 , 过滤 |
| D | 除去铝粉中的铜粉 | 加适量稀硫酸,过滤 |





①原子的数目 ②分子的数目 ③元素的种类 ④物质的种类
⑤原子的种类 ⑥原子的质量 ⑦元素的化合价 ⑧分子的种类




Ⅰ.取少量固体样品于烧杯中,先加足量水溶解,再加入足量的BaCl2溶液,有白色沉淀产生;
Ⅱ.继续向烧杯中滴加稀盐酸并不断搅拌,烧杯内固体质量随加入稀盐酸质量的变化如图所示。请回答下列问题:

[提出问题 1] 该氢氧化钠溶液是否变质了呢?
[实验探究 1]
|
实验操作 |
实验现象 |
实验结论 |
|
取少量该溶液于试管中,向溶液中滴加足量的稀盐酸,并不断振荡 |
|
氢氧化钠溶液一定变质了。 |
[提出问题 2] 该氢氧化钠溶液是全部变质还是部分变质呢?
[猜想与假设]
猜想 1:氢氧化钠溶液部分变质。猜想 2:氢氧化钠溶液全部变质。
[实验探究 2]
|
实验步骤 |
实验现象 |
实验结论 |
|
⑴取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡。 |
有白色沉淀生成。 |
说明原溶液中一定有碳酸钠。 |
|
⑵取步骤(1)试管中的少量上层清液,滴加酚酞溶液。 |
溶液变红色。 |
说明原溶液中一定有。 |
[实验结论]该氢氧化钠溶液部分变质。猜想 2 正确。
[思考与讨论]有同学认为,探究 1 已经证明了碳酸钠的存在,所以实验探究 2 中的实验步骤(1)是多余,只要如实验步骤(2),样品溶于水后,直接滴入酚酞即可的。该同学的看法是否正确?为什么?。

主要实验步骤如下:
I.打开弹簧夹,对装置A通一段时间的氮气;
II.把装置A连接上装置B、C、D,关闭弹簧夹,给碳酸氢铵样品加热;
III.当样品反应完全,……,再停止加热,直到玻璃管冷却;
Ⅳ.实验完毕,测得装置B、C中药品的质量分别增加了m1、m2。
Ⅳ.根据实验数据m1、m2 , 算出该样品中碳酸氢铵的质量分数。
请回答下列问题:
①SiO2+2C Si+2CO↑ ②Si+2Cl2
SiCl4 ③SiCl4+2H2
Si+4HCl



①取质量、大小相同的 3 个烧杯,分别加入一定质量分数的稀盐酸 100 克;
②向上述 3 个烧杯中分别加入 3 份质量不同的样品;
③充分反应后,再用电子天平称量烧杯及烧杯内物质的总质量(假设产生的气体完全逸出)。实验数据记录如下:
|
实验一 |
实验二 |
实验三 |
|
|
反应前稀盐酸+烧杯质量(克) |
150 |
150 |
150 |
|
反应前固体样品质量(克) |
4 |
8 |
12 |
|
反应后烧杯内物质+烧杯质量(克) |
m |
155.8 |
158.7 |
![]()