 B . 稀释浓硫酸
B . 稀释浓硫酸  C . 闻食醋
C . 闻食醋  D . 检查装置气密性
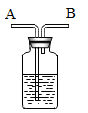
D . 检查装置气密性 
| 选项 | A | B | C | D |
| 类别 | 酸 | 碱 | 盐 | 氧化物 |
| 实例 | 硝酸、盐酸 | 熟石灰、烧碱 | 食盐、纯碱 | 水、高锰酸钾 |



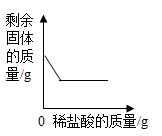 B .
B . 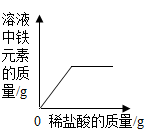 C .
C . 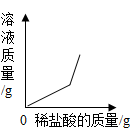 D .
D . 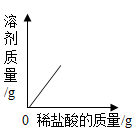

①食盐 ②熟石灰 ③稀盐酸 ④小苏打 ⑤甲烷


【实验目的】确定白色固体的组成
【实验方案】
【实验结论】该白色固体由NaHCO3和NaCl两种物质组成
由此同学们总结得出:复分解反应发生的条件是有沉淀或气体或水生成。


【查阅资料】①铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液;
②铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜。铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液。
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮。
|
实验一 |
实验二 |
实验三 |
|
|
实验 方案 |
| | |
| 实验 现象 | 铬片表面产生气泡缓慢,溶液变蓝色。 | 无现象 | 铝片表面产生气泡较快。 |
| 结论 | 铬能和稀硫酸发生反应,反应速率较慢。 | 铜不与稀硫酸反应 | 铝能与稀硫酸反应,反应速率较快。 |
| 三种金属在金属活动性顺序中的相对位置关系是 | |||
【回答问题】



|
装置丙 |
装置丁 |
|
|
反应前 |
48.8克 |
161.2克 |
|
反应后 |
46.5克 |
163.9克 |
小明根据装置丙减少的质量就是氧元素质量,求得氧化铜质量为11.5克,纯度为76.7%。小丽想根据装置丁的质量变化进行计算,请帮小丽求出氧化铜样品的纯度(写出计算过程)。
