 B .
B .  C .
C .  D .
D . 

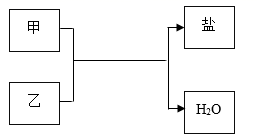
| 选项 | 甲 | 乙 |
| A | Fe2O3 | 稀硫酸 |
| B | SO3 | NaOH溶液 |
| C | 稀盐酸 | Ca(OH)2溶液 |
| D | 稀盐酸 | AgNO3溶液 |

此“最简单”反应中, 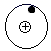 表示H原子,
表示H原子,  表示D原子。
表示D原子。
D原子核中有个质子,此反应中涉及的元素种类有种。该反应可表示为H+→H2+
(实验方案)取研细和干燥后的木炭(0.3g)和CuO(2.0g),混合均匀并装入试管,连接装置,高温反应,检验气体。
(实验过程)
由如图装置③中粉末的颜色变化可检验CO,除此之外,还可通过几种装置的组合,由另一种明显的现象来进一步确定CO的存在,则装置连接的最佳顺序为________→尾气处理(填字母)。
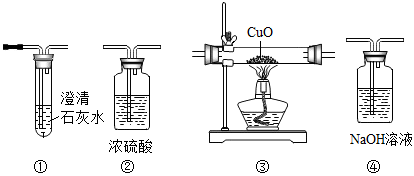
(实验结论)高温下,过量木炭还原CuO的气体产物中有CO。
(延伸应用)冬天,室内用炭火取暖时,应注意。

|
溶液的pH |
6.0 |
6.5 |
7.0 |
7.5 |
8.0 |
9.0 |
|
产物颜色 |
黄褐色 |
黄褐色 |
较黑 |
很黑 |
很黑 |
灰黑色 |
|
产率(%) |
43.9 |
50.6 |
86.2 |
93.0 |
92.3 |
91.6 |

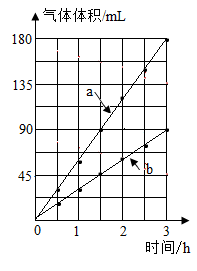
| 试验编号 | H2O2的质量分数(%) | H2O2溶液的体积(mL) | 对应曲线 |
| Ⅰ | 3.4 | 10.0 | a |
| Ⅱ | 2.4 | 10.0 | b |
| Ⅲ | 1.7 | 10.0 | c(待绘制) |