
 把NaOH和NH4NO3固体分别溶于水中
B .
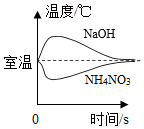
把NaOH和NH4NO3固体分别溶于水中
B . 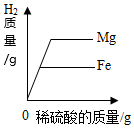 分别向等质量镁和铁中,逐渐加入溶质质量分数相同的稀硫酸至过量
C .
分别向等质量镁和铁中,逐渐加入溶质质量分数相同的稀硫酸至过量
C . 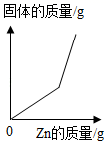 向一定质量硝酸银的混合溶液中逐渐加入锌粉
D .
向一定质量硝酸银的混合溶液中逐渐加入锌粉
D . 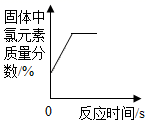 加热一定质量氯酸钾和二氧化锰的固体混合物
加热一定质量氯酸钾和二氧化锰的固体混合物
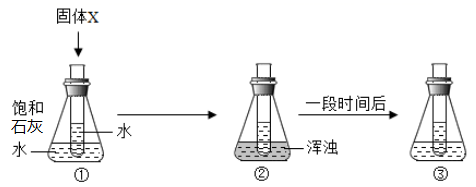
| 溶剂 | 氢氧化钠 | 碳酸钠 | ||
| 20℃ | 40℃ | 20℃ | 40℃ | |
| 水 | 109g | 129g | 21.8g | 49g |
| 酒精 | 17.3g | 40g | 难溶 | 难溶 |
下列有关分析和推理错误的是( )
|
温度/℃ |
10 |
20 |
30 |
40 |
|
|
溶解度/g |
氯化钠 |
35.8 |
36.0 |
36.3 |
36.6 |
|
碳酸钠 |
12.2 |
21.8 |
39.7 |
53.2 |
|
①40℃时,氯化钠的溶解度为g.
②碳酸钠的溶解度随温度的升高而(填“增大”或“减小”).在20℃时,将100g的水加入30g碳酸钠中,充分搅拌后得到的是(填“饱和溶液”或“不饱和溶液”),将上述溶液升温到30℃,该溶液的溶质质量分数为 (计算结果精确到0.1%).
③10℃时,分别配制表中两种物质的饱和溶液,其中溶质质量分数较小的物质是.


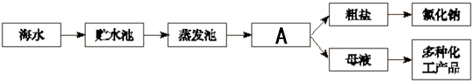
①氯化钠固体不纯
②称量时,砝码端忘垫质量相同的纸片
③量取水时,仰视读数
④装瓶时,有少量溶液洒出
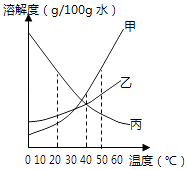
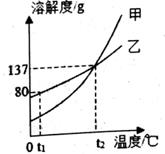
①20℃时,甲的溶解度(填“>”、“<”或“=”)乙的溶解度.
②40℃时,乙和丙(填“能”或“不能”)形成溶质质量分数相同的饱和溶液.
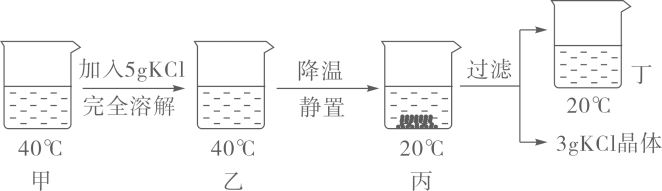
③20℃时,烧杯中分别盛有相同质量甲、乙、丙的饱和溶液,各加入等质量的对应固体,并升温至50℃.请填写下表.
烧杯中的溶质 | 烧杯中固体的变化 |
甲 | 固体逐渐 |
乙 | 固体逐渐 |
丙 | 固体逐渐 |
打开可乐瓶,逸出大量气泡.由此可见,压强越小,CO2的溶解度越.为增大CO2的溶解度,可采用的一种方法是.