 B . 收集二氧化碳
B . 收集二氧化碳  C . 测定溶液pH
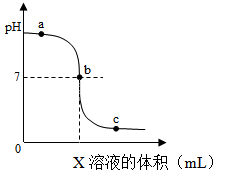
C . 测定溶液pH  D . 制备O2发生装置
D . 制备O2发生装置 
![]()
| 食物 | 柠檬汁 | 橙子汁 | 西瓜汁 | 鸡蛋清 |
| pH | 2.2~2.4 | 3.6~4.3 | 5.3~6.1 | 7.6~8.0 |
下列说法中正确的是( )
 B .
B .  C .
C .  D .
D . 

步骤1:从A处通入空气,点燃酒精灯,观察到硫粉熔化、燃烧,产生微弱的淡蓝色火焰;
步骤2:从A处改通入氧气,观察到硫燃烧产生明亮的蓝紫色火焰。
下列说法错误的是( )
实验一:室温时,将蒸馏水和不同pH的硫酸、氢氧化钠溶液,放入14支试管中,分别向每支试管中滴加3滴黑枸杞提取液。实验结果如下:
|
pH |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
|
颜色 |
粉红 |
粉红 |
粉红 |
浅紫 |
浅紫 |
紫 |
紫 |
蓝 |
蓝 |
深蓝 |
深蓝 |
灰绿 |
黄 |
黄棕 |
实验二:室温时,向试管中分别加入相同体积的4种物质,各滴加3滴黑枸杞提取液。
实验结果如下:
|
物质 |
稀盐酸 |
牛奶 |
蒸馏水 |
炉具清洁剂 |
|
颜色 |
粉红 |
紫 |
紫 |
黄 |
回答下列问题:
黑枸杞提取液在pH=6,pH=7的溶液中均会变紫,故不能确定牛奶呈中性,还可能
①氢氧化钠固体表面出现液体是因为氢氧化钠吸收空气中的水分而潮解。
②电子天平示数增加的原因除了吸收水分以外,还有另一个原因是(用化学方程式表示)。
(作出猜想)猜想一:有氢氧化钠
猜想二:没有氢氧化钠
(查阅资料)BaCl2溶液、NaNO3溶液、Ba(NO3)2溶液均呈中性。
(进行实验)小明同学取少量烧杯中的溶液于试管中,滴入几滴无色酚酞,观察到溶液变红,小明同学认为猜想一成立。
(交流与评价)小玲同学认为小明同学的结论不一定正确,原因是。于是,小玲同学继续进行探究。
|
实验操作 |
实验现象 |
实验结论 |
|
小玲同学在小明同学所做实验后的溶液中,滴入足量的Ba(NO3)2溶液 |
|
猜想一成立 |
①根据氢氧化钠固体易潮解的性质,可用氢氧化钠固体作某些气体的。
②另取少量烧杯中的溶液进行以下实验,也能证明猜想一成立的是(填序号)。
A 先加足量稀盐酸,再滴加紫色石蕊溶液
B 先加足量BaCl2溶液,静置,取上层清液,再滴加CuCl2溶液
C 先加足量Ca(OH)2溶液,静置,取上层清液,再滴加酚酞溶液
D 先加足量Ba(NO3)2溶液,静置,取上层清液,再滴加FeCl3溶液
(认识组成)由化学式Na2CO3、NaHCO3可知,两者含有的元素差别是;从构成离子的层次看,酸根离子分别是CO 、HCO
,根据酸根离子,他们都可统称为(填碳酸盐或钠盐)。
(比较性质)为比较室温是20℃时Na2CO3、NaHCO3与水混合的变化,按如图进行实验,先向两支试管中分别加入约1克Na2CO3、NaHCO3 , 再分别滴入几滴水,震荡后将温度计插入其中,发现盛有Na2CO3的试管中温度计的示数高于20℃,盛有NaHCO3的试管中温度计的示数低于20℃,再向两试管中各加入约五毫升水和两滴酚酞试液震荡后,液体均呈红色。则NaHCO3与水混合时(填放出或吸收热量),NaHCO3溶液显(填酸性或碱性)。

(提出问题)Na2CO3、NaHCO3还有什么不同性质?
(查阅资料)NaHCO3受热易分解生成Na2CO3、H2O和CO2 , Na2CO3受热不易分解。可用如图装置验证。
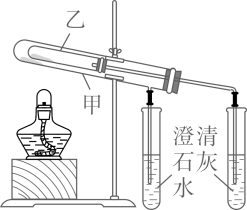
(进行实验)按上图链接装置,检查气密性后,分别装入相关药品(试管甲、乙中的固体质量应相等)。后续试验均按规范要求进行,完成实验。
①若要使实验效果更理想,则甲中应装入(填Na2CO3或NaHCO3)
②完成试验后,待试管冷却至室温,加甲、乙试管里剩余固体的质量分别用m(甲)、m(乙)表示,则m(甲)(填>或<或=)m(乙)
(拓展应用)①若把碳酸和NaHCO3比较,受热容易分解的是(填碳酸或NaHCO3),除去Na2CO3粉末中混有的少量NaHCO3的方法是。
②研究表明Na2CO3在水中溶解时能生成自由移动的离子,且Na2CO3溶液中还含有很少的HCO 离子,在Na2CO3溶液中存在的带负电荷的离子有HCO
、、(填离子符号)。


求: