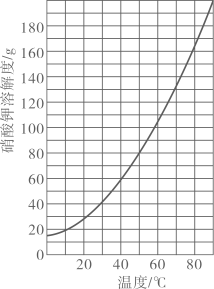
| 选项 | 操作 | 溶质质量 | 溶液质量 | 溶质的质量分数 | KNO3的溶解度 |
| A | 升温 | 变大 | 变大 | 不变 | 变大 |
| B | 降温 | 变小 | 变小 | 不变 | 变小 |
| C | 加入KNO3固体 | 不变 | 变大 | 变大 | 变大 |
| D | 恒温蒸发部分水 | 变小 | 变小 | 不变 | 不变 |
物质b的溶解度表
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| b的溶解度/g | 14 | 20 | 30 | 45 | 65 | 85 | 110 |
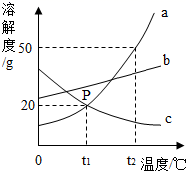
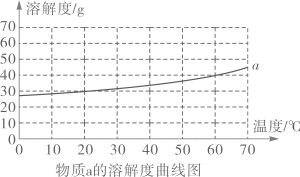
①所有物质的溶解度都随温度的升高面增大
②30℃时,物质的溶解度a小于b
③物质b中含有少量a时,可以采用降温结晶的方法提纯b
④40℃时,分别将物质a、b的饱和溶液降温至10℃,析出物质的质量b大于a

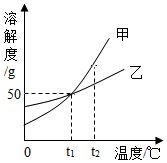
①a>b ②a<b ③a=b ④均有可能

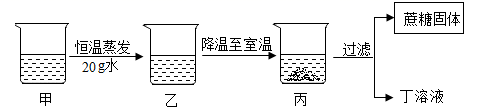
若70gNH4H2PO4中混有5 g NaCl杂质,可按照以下步骤进行除杂。
①在℃下,用100g水溶解,确保固体刚好完全溶解。
②将①的饱和溶液降温到10℃时,溶液中析出 NH4H2PO4的质量应为g。
③再进行过滤、(填操作名称)、干燥,即可得到较纯净的NH4H2PO4。
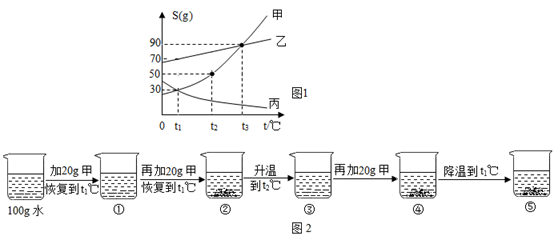
A 在溶液①~⑤中,属于饱和溶液的是②④⑤
B 与溶液②溶质质量分数相等的是⑤
C 杯④中所得溶液的质量为160g
D 烧杯⑤中固体的质量为30g
(资料)①K2CO3 + Ca(OH)2 = CaCO3↓ + 2KOH
②Ca(OH)2、K2CO3 和 KOH 的部分溶解度如下表:
|
温度/℃ |
0 |
10 |
20 |
30 |
50 |
|
|
溶解度/g |
Ca(OH)2 |
0.18 |
0.17 |
0.16 |
0.15 |
0.14 |
|
K2CO3 |
107 |
109 |
110 |
114 |
121 |
|
|
KOH |
97 |
103 |
112 |
126 |
140 |
|
a溶质的质量 b溶质的质量分数 c 氢氧化钙的溶解度 d溶剂的质量 e溶液的质量
|
实验序号 |
① |
② |
③ |
④ |
|
加入氯化钠的质量/g |
9 |
36 |
81 |
90 |
|
溶液质量/g |
209 |
236 |
272 |
272 |
若将②中得到的溶液稀释成质量分数为 0.9%的生理盐水,需加水的质量是g。关于上述实验的叙述正确的是(填序号)。
a①②所得溶液是不饱和溶液
b③④所得溶液中,溶质的质量分数相等
c20℃时,200 g 水中最多溶解氯化钠的质量为 72 g
d20℃时,将④继续恒温蒸发 100 g 水,过滤,得到质量为 36 g 的固体