①溶质质量 ②溶剂质量 ③溶液质量 ④溶质质量分数 ⑤溶解度
①称量的氯化钠固体中含有不溶性杂质; ②用量筒量取水时仰视读数;
③往烧杯中加水时有水洒出; ④将配制好的溶液装入试剂瓶中时有少量溅出。

温度/℃ | 0 | 10 | 20 | 30 | 40 | |
溶解度/g | NaCl | 35.0 | 35.5 | 36.0 | 36.5 | 37.0 |
Na2CO3 | 6.0 | 10.0 | 18.0 | 36.5 | 50.0 | |

①计算:需要Na2CO33.0g,水47.0g
②称量:用托盘天平称量3.0g的Na2CO3。天平调零后,分别在天平左右托盘放上质量相同的纸片,先,然后,至托盘天平恰好平衡。
③量取:用量筒量取47.0 mL水。请在图中画出47.0 mL水的液面位置。
![]() 。
。
④溶解。
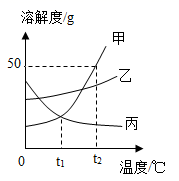
At1℃甲、乙两物质溶液的溶质质量分数相等
Bt2℃配制300g甲的饱和溶液,需要固体甲的质量为100g
Ct2℃甲、乙、丙三种饱和溶液降温到t1℃,甲析出晶体的质量比乙多
Dt1℃等质量的甲、乙、丙三种固体配制成该温度下的饱和溶液,所得溶液的质量大小:丙>甲=乙。


|
实验次数 |
加入稀盐酸的质量/g |
剩余固体的质量/g |
|
1 |
20 |
15 |
|
2 |
20 |
10 |
|
3 |
20 |
6.8 |
|
4 |
20 |
n |