| 物质 | 分子个数 | 体积 | ||
| 0℃/101 kPa | 20 ℃/101 kPa | 0℃/202 kPa | ||
| 17 g 氨气 | 约6.02×1023个 | 22.4L | 24.1L | 11.2L |
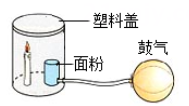
 B . 比较火焰各层温度
B . 比较火焰各层温度  C . 验证质量守恒定律
C . 验证质量守恒定律  D . 验证产物有水
D . 验证产物有水 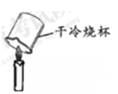
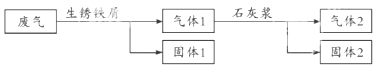
①用生锈铁屑处理废气中的CO,体现CO性。
②用石灰浆不用石灰水的原因是
③固体2中有(写两种物质)。
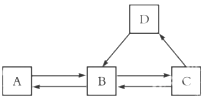
①B转化为A的化学方程式为
②若D广泛用于玻璃、洗涤剂的生产,则D转化为B的基本反应类型是
检验D中阴离子的方法是
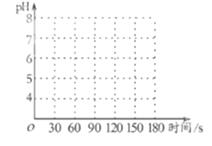
③将足量C通入石蕊溶液中,现象是;该溶液pH=4,加热至90s时C完全排出,画出加热过程pH变化图像。
④硝酸钾可作化肥,能供给作物两种养分,属于肥料
【提出问题】铁锈蚀与哪些因素有关?
【查阅资料】
①氯化钙固体可作干燥剂。
②一定条件下,碳可加快铁的锈蚀,但碳本身不参加反应。
③常温常压,氢气密度是dg/mL.
【设计与实验】
实验一:定性探究铁锈蚀的因素
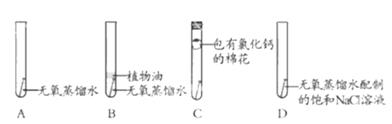
取四枚相同的洁净无锈铁钉分别放入试管,进行图1实验,现象如表1.
|
试管 |
一周后现象 |
|
A |
铁钉表面有一层铁锈 |
|
B |
铁钉表面无明显变化 |
|
C |
铁钉表面无明显变化 |
|
D |
铁钉表面有较厚铁锈 |
小组设计了图2装置,检查气密性,将5g铁粉和2g碳粉加入三颈烧瓶,t,时刻加入2mL饱和NaCl溶液后,再将一只装有5mL稀盐酸的注射器插到烧瓶上,采集数据。

据图3,t2时刻后反应并未停止温度却开始降低,原因是

将实验二烧瓶中剩余物质过滤、洗涤、干燥,得mg固体,连接图5装置,检查气密性,加入固体与足量稀盐酸进行实验。
完全反应后,常温常压下测得生成气体体积为VmL,则该固体中铁锈质量分数表达式为
与实验一对比,实验二铁锈蚀明显更快的原因是