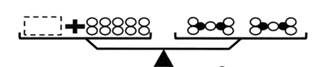
| 物质 | X | Y | Z | W |
| 反应前的质量/g | 20 | m | 16 | 14 |
| 反应后的质量/g | 4 | 6 | 60 | 50 |



| 物 质 | A | B | C | D |
| 反应前的质量/g | 1.4 | 7 | 31.6 | 0 |
| 反应后的质量/g | 待测 | 26.7 | 0 | 3.2 |
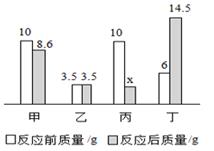
| 物质 | 苯 | 氧气 | 二氧化碳 | 水 | X |
| 反应前的质量(g) | 3.9 | 9.6 | 0 | 0 | 0 |
| 反应后的质量(g) | 0 | 0 | 6.6 | 2.7 | m |
|
第一次 |
第二次 |
第三次 |
|
|
O2的质量(g) |
3 |
4 |
6 |
|
SO2的质量(g) |
6 |
8 |
8 |


![]()
则步骤①、②发生反应的化学方程式是分别是、。

①取质量、大小相同的3个烧杯,分别加入一定质量分数的稀盐酸100克;
②向上述3个烧杯中分别加入3份质量不同的样品;
③充分反应后,再用电子天平称量烧杯及烧杯内物质的总质量(假设产生的气体完全逸出)。实验数据记录如下:
| 实验一 | 实验二 | 实验三 | |
| 反应前稀盐酸+烧杯质量(克) | 150 | 150 | 150 |
| 反应前固体样品质量(克) | 4 | 8 | 12 |
| 反应后烧杯内物质+烧杯质量(克) | m | 155.8 | 158.7 |
已知实验中发生的化学反应: NaOH+HCl=NaCl+H2O;Na2CO3+2HCl=2NaCl+H2O+CO2↑
|
第一次 |
第二次 |
第三次 |
|
|
O2的质量(g) |
3 |
4 |
6 |
|
SO2的质量(g) |
6 |
8 |
8 |
|
物质 |
第一份 |
第二份 |
第三份 |
第四份 |
|
反应前A的质量(克) |
11 |
8 |
a |
|
|
反应前B的质量(克) |
1 |
4 |
b |
|
|
反应后生成C的质量(克) |
5 |
10 |
7.5 |
|
物质 |
第一份 |
第二份 |
第三份 |
第四份 |
|
反应前A的质量(克) |
11 |
8 |
a |
|
|
反应前B的质量(克) |
1 |
4 |
b |
|
|
反应后生成C的质量(克) |
5 |
10 |
7.5 |
猜想一:生成的气体可能是氧气。
猜想二:生成的气体可能是氢气。
为验证生成的气体是什么,该组同学在老师的指导下,设计了如图所示的实验装置,并收集反应产生的气体(装置中必要的铁架台、铁夹、铁圈、石棉网、加热设备等在图中均已略去)。试管A内装有铁粉,烧瓶B中装有一定量的水,提供反应所需的水蒸气。

【提出问题】化学反应前后各物质的质量总和是否相等?
【猜想与假设】猜想1:可能不相等; 猜想2:可能相等。
【实验探究】甲、乙两组同学用托盘天平分别称量反应前后物质的质量。
|
甲组 |
乙组 |
|
|
实验方案(反应后略) |
|
|
|
实验现象 |
有气泡产生,天平指针向右偏转 |
铁钉表面有红色物质析出,溶液颜色发生改变,天平指针没有偏转 |
|
结论 |
猜想1正确 反应的化学方程式:_ |
猜想2正确 |
【反思评价】究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体溢出,导致指针向右偏转。得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应一定要在密闭中进行。
【优化装置】同学们对甲组左盘中的反应装置进行了如下三种改进,你认为最佳装置是(2)(填序号),从另外两种装置中任选一种指出其不足(3)。

[提出猜想]小红猜想是氧气;小敏猜想是氢气;小雨猜想是
二氧化碳。其他同学认为小雨的猜想是错误的,理由是;
[进行实验]利用图Ⅰ所示的装置分别进行实验
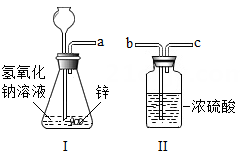
⑴小红:反应一段时间后,将带火星的木条放在a处,观察到木条不复燃,则她的猜想错误。
⑵小敏:①用图Ⅱ所示装置干燥从a导管出来的气体,将管口a与(填“b”或“c“)端管口连接。
②反应一段时间,点燃干燥的气体,通过对现象的分析,得出他的猜想正确。
[得出结论]锌和氢氧化钠反应生产氢气和偏铝酸钠(Na2ZnO2),反应的化学方程式为:。
[交流讨论]有同学认为,小敏的实验方案有欠缺,步骤②中存在安全隐患,理由是。

2CuS+3O2 2CuO+2SO2
Cu2S+O2 CuO+SO2(没配平)
请写出后两个实验步骤:
实验步骤二:。
实验步骤三:。