![]()
![]()
![]()
 B . 氢气还原氧化铜
B . 氢气还原氧化铜  C . 加热液体
C . 加热液体  D . 稀释浓硫酸
D . 稀释浓硫酸 

 B . 向硫酸和氯化镁混合溶液中滴加过量的氢氧化钠溶液
B . 向硫酸和氯化镁混合溶液中滴加过量的氢氧化钠溶液  C . 将足量镁粉和铝粉分别与等质量同浓度的稀硫酸反应
C . 将足量镁粉和铝粉分别与等质量同浓度的稀硫酸反应  D . 向盛有一定量稀硫酸的烧杯中不断加入蒸馏水
D . 向盛有一定量稀硫酸的烧杯中不断加入蒸馏水 
| 加入的物质 | 酚酞试液 | Fe2O3粉末 | BaCl2溶液 |
| 实验现象 | 无明显现象 | 固体逐渐溶解,溶液变黄 | 无明显现象 |


| 选项 | 待鉴别的物质 | 鉴别方法 |
| A | 水、过氧化氢溶液 | 加二氧化锰,观察能否产生气体 |
| B | 食盐水、盐酸 | 加入无色酚酞试液,观察溶液颜色的变化 |
| C | 硝酸铵、氢氧化钠 | 加水溶解,用手触摸烧杯外壁,感知温度的变化 |
| D | 棉纤维、羊毛纤维 | 点燃,闻燃烧产生的气体气味 |
②向滤液中加入稀盐酸,一定有沉淀产生。 ③滤渣中一定含有Ag,可能有Fe。 ④滤液中一定含有Fe(NO3)2 , 一定不含AgNO3 , 可能含有Al(NO3)3。以上说法正确的个数为( )
 化学能→电能
B .
化学能→电能
B .  电能→机械能
C .
电能→机械能
C .  光能→化学能
D .
光能→化学能
D .  机械能→内能
机械能→内能
 人用力搬石头没有搬动
B .
人用力搬石头没有搬动
B .  人将货物从地面拉到高处
C .
人将货物从地面拉到高处
C .  人推一块大石头没推动
D .
人推一块大石头没推动
D .  人使箱子沿水平方向做匀速直线运动
人使箱子沿水平方向做匀速直线运动
 B . 开瓶器
B . 开瓶器  C . 筷子
C . 筷子  D . 船桨
D . 船桨 

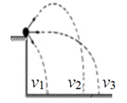
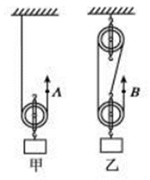

 B .
B .  C .
C .  D .
D . 
①氢气 ②胆矾 ③熟石灰 ④碳酸氢铵 ⑤硫酸钾 ⑥烧碱 ⑦一氧化碳
则步骤①、②发生反应的化学方程式是分别是、。



【提出问题】甲烷燃烧后可能生成哪些物质?
【猜想假设】甲同学:CO2 H2O;乙同学:CO H2O;丙同学:CO2 CO H2O。
【实验探究】将甲烷在一定量的纯净氧气中燃烧产物依次通过下列装置,进行验证。


已知:A中发生的反应为:H2SO4(浓)+Na2SO3=Na2SO4+SO2↑+H2O
B中发生的反应为:Na2SO3+SO2=Na2S2O5
【相关资料】①淡黄色固体是过氧化钠(Na2O2)。
②吹出的气体主要成分有氮气、二氧化碳和水蒸气。
③过氧化钠与氮气不反应。
【分析讨论】根据棉花团剧烈燃烧的现象推测,反应中除了生成氧气外,还说明过氧化钠发生的相关化学反应是(填“吸热”或“放热”)反应。
【提出猜想】同学们发现残留固体呈白色,对该固体成分进行猜想:
猜想Ⅰ:只有CO2与Na2O2反应,固体成分是Na2CO3。
猜想Ⅱ:只有H2O与Na2O2反应,固体成分是NaOH。
猜想Ⅲ:CO2和H2O都与Na2O2反应,固体成分是Na2CO3和NaOH的混合物Na2CO3与NaOH的混合物。
【实验探究】同学们在老师带领下用足量潮湿的CO2气体通入过氧化钠粉末中,充分反应后,取白色固体于试管中配成溶液,设计实验对猜想进行验证。
验证Ⅰ:取少量溶液滴加稀盐酸,发现有气泡产生.有同学认为固体成分仅含Na2CO3。
验证Ⅱ:蘸取少量溶液滴到pH试纸上,测得pH大于7,有同学认为固体只有NaOH。
验证Ⅲ:另取少量溶液先加入溶液,有白色沉淀产生,静置后向上层清液滴加酚酞酚酞试液,上清液显红色,从而验证了猜想Ⅲ是正确的。
【实验反思】验证Ⅰ的结论错误,因为它不能排除的存在。验证Ⅱ的结论错误,因为。

|
实验次数 |
物重G/N |
物体上升高度h/m |
拉力F/N |
拉力作用点移动距离s/m |
机械效率η/% |
|
1 |
1 |
0.1 |
0.7 |
0.3 |
47.6 |
|
2 |
1 |
0.2 |
0.7 |
0.6 |
47.6 |
|
3 |
2 |
0.1 |
1.1 |
0.3 |
60.6 |
|
4 |
4 |
0.1 |
2 |
0.3 |
① |