 D . 氧化镁中镁元素的化合价:
D . 氧化镁中镁元素的化合价: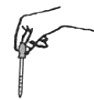 滴加试剂
B .
滴加试剂
B . 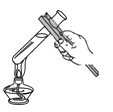 加热液体
C .
加热液体
C . 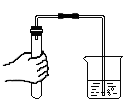 检查气密性
D .
检查气密性
D .  闻气体气味
闻气体气味


实验1:向两支试管中分别加入0.2 g Ca(OH)2粉末,然后各加入2 mL水,振荡后静置,试管底部有粉末,溶液呈无色。
实验2:向两支试管中再各滴入2滴酚酞溶液,振荡后静置,溶液由无色变为红色,试管底部粉末无明显变化。
实验3:继续向其中一支试管中加入2 mL水,振荡后静置,无明显变化;向另一只试管中加入2 mL稀盐酸,振荡后静置,溶液由红色变为无色,试管底部的粉末消失。
下列说法正确的是( )
温度/℃ | 95 | 90 | 80 | 30 | 10 |
析出M的质量/g | 0 | 0 | 15 | 100 | 116 |
选项 | 实验目的 | 操作 |
A | 干燥CO2气体 | 将气体通过碱石灰(NaOH和CaO的混合物) |
B | 除去NaCl溶液中含有的少量Na2CO3杂质 | 向NaCl溶液中加入适量的Ca(NO3)2溶液,过滤 |
C | 鉴别NH4Cl和KCl两种化肥 | 取两种化肥,分别加入少量熟石灰粉末,混合研磨,闻气味 |
D | 配制5%的KNO3溶液 | 向盛有5g KNO3固体的烧杯中,加入100mL蒸馏水,搅拌 |


报道一:在一定条件下,利用太阳能可将CO2热解为碳和氧气;
报道二:2021年9月23日中科院新闻发布会上,介绍了天津工业生物技术研究所首次实现从CO2到淀粉分子的全合成,这一科研成果使淀粉生产从传统农业种植模式转向工业车间生产模式成为可能,是颠覆性的技术新突破。

a.植树造林 b.燃煤供暖 c.风力发电
a.使用可降解塑料 b.露天焚烧废旧塑料 c.直接填埋废弃塑料
a.纯碱 b.硝酸 c.明矾




①鼓入足量空气能使木炭从而提高炉温。
②炼锡时,有关键的一步“点铅勾锡”,即加铅能使锡较易熔化流出,其原因是。
①锡往往与其它金属制成合金使用,目的是(选填 “增大”或“减小”)硬度。
②古代锡器常用来饮酒喝茶,很少装酸性物质,原因是。

i、2KClO3+2MnO2=2KMnO4+Cl2↑+O2↑
ii、KMnO4分解产生K2MnO4、MnO2和O2
iii、Cl2+K2MnO4=2KCl+MnO2+O2
①发生装置应选用(填字母)。
②反应ii的化学方程式为。
③反应中MnO2的作用是。


【实验过程】步骤1 在通风橱中,按上图连接装置并检验装置的气密性。
步骤2 装入试剂:玻璃管内装入Fe2O3粉末,试管Ⅰ中装入澄清石灰水。
步骤3 从a端通入CO一段时间,待排尽空气后,再点燃酒精灯。
【实验现象】反应一段时间后,玻璃管内粉末由色变成黑色,生成的黑色固体均能被玻璃管上方的磁铁吸引。试管Ⅰ中出现白色沉淀(用化学反应方程式表示:)。
【查阅资料】铁粉、FeO、Fe3O4均为黑色固体;铁粉、Fe3O4均能被磁铁吸引。
【提出猜想】对磁铁吸引的黑色固体成分有以下三种猜想:
猜想Ⅰ:Fe;猜想Ⅱ:Fe3O4;猜想Ⅲ:Fe和Fe3O4
【实验验证】取少量反应后的黑色固体放入试管中,加入足量的硫酸铜溶液,振荡,充分反应后静置,观察到红色固体中混有黑色颗粒,说明(填“猜想Ⅰ”、“猜想

Ⅱ、原料气CO的制备
方法一:加热MgCO3、Zn的混合物可快速制备CO,同时还得到两种金属氧化物:、(填化学式)。
方法二:加热草酸晶体(H2C2O4·2H2O)制备CO:H2C2O4·2H2OCO↑+CO2↑+3H2O
已知:常压下,草酸晶体的熔点为101℃,比较草酸晶体的熔点和分解温度,分析若选用如图装置Ⅲ制备装置Ⅰ所需的CO,可能存在的问题是。


①“滤渣”中含有(填化学式)。
②“操作X”的名称为。
步骤1 称取一定质量的NaCl,加水溶解。
步骤2 向其中加入一定质量的NH4HCO3 , 充分反应。
步骤3 过滤、洗涤、干燥、加热可得Na2CO3。
已知:NaHCO3受热易分解:2NaHCO3Na2CO3+H2O+CO2↑。
相关物质的溶解度曲线如图所示。

①步骤2中反应的化学方程式为。
②图10中碳酸氢铵溶解度在30 ℃后无数据的原因可能是。
Ⅰ定性分析
称取m1 g 晶体,利用如图装置(夹持仪器略)分析晶体的成分。

①反应一段时间后,能说明晶体中含有NaHCO3的现象为。
②将晶体加热至残留固体的质量不再改变,测得残留固体的质量为m2 g。若1∶1<m1∶m2 <,也能说明晶体中含有NaHCO3。
③甲同学认为通过测定装置B中沉淀的质量,即可确定晶体的组成。请对甲同学的观点进行评价:。
Ⅱ定量分析
步骤1:取2.500 g晶体于锥形瓶中,加水使样品完全溶解。向锥形瓶中逐滴滴加溶质质量分数为1%的稀盐酸,当Na2CO3恰好完全转化为NaHCO3时,发生反应的化学方程式为:Na2CO3+HCl=NaHCO3+NaCl,反应消耗稀盐酸83.19 g。
步骤2:向步骤1所得的溶液中继续逐滴滴加溶质质量分数为1%的稀盐酸,至NaHCO3恰好完全反应时,发生反应的化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑,又消耗稀盐酸86.84 g。
④晶体中NaHCO3的质量分数为(写出计算过程)。
⑤乙同学认为做完步骤1即可确定晶体的组成。请对乙同学的观点进行评价:。