|
商品 |
|
|
|
|
|
选项 |
A.玉器 |
B.丝绸 |
C.铁器 |
D.纸张 |


|
选项 |
A |
B |
C |
D |
|
装置 |
|
|
|
|
|
操作及目的 |
煅烧贝壳至900℃,得到生石灰 |
浓缩海水,加生石灰反应后过滤,得到 |
蒸发 |
电解 |
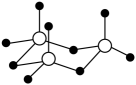 )中含有σ键数目为6 NA
C . 绿矾分解生成16g
)中含有σ键数目为6 NA
C . 绿矾分解生成16g


(注:−表示电极电位曲线;…表示pH曲线)
已知:酸性介质中,1mol/L不同电对的电极电势见下表。电极电势越高,其氧化型物质的氧化性越强;电极电势越低,其还原型物质的还原性越强。
|
电对(氧化型/还原型) |
|
|
|
|
|
|
电极电势 |
0.771 |
1.776 |
0.695 |
1.224 |
0.536 |
回答下列问题:
催化
分解反应过程包括i、ii两步:
反应i: (未配平)
反应ii:
反应i的离子方程式为。
用可逆反应设计电池,按图a装置进行实验,测得电压E(
)随时间t的变化如图b所示:

电池初始工作时,正极的电极反应式为。
猜想1:增大,
的氧化性减弱,正极的电极电势降低。
猜想2:减小,
的氧化性增强,负极的电极电势升高。
①时间后,按图a装置探究,验证上述猜想的合理性,完成表中填空。
|
实验 |
实验操作 |
电压E/V |
结论 |
|
i |
往烧杯A中加入适量Fe |
E0 |
猜想1成立 |
|
ii |
往烧杯B中加入适量 |
E<0 |
猜想2成立 |
②有同学认为,上述实验不足以证明猜想1成立。利用上述反应,从化学平衡移动的角度解释猜想1不足以成立的理由。
③为进一步验证猜想1,进行实验Ⅱi,完成表中填空。
|
实验 |
实验操作 |
电压E/V |
结论 |
|
iii |
往烧杯A中加入适量 |
E<0 |
猜想1成立 |
结论:可逆氧化还原反应中,浓度的变化引起电对氧化性变化,从而改变电池反应方向。

已知:①“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有、
。
②“酸浸”时,锑元素反应生成难溶的浸渣。
回答下列问题:
A. B.
C.
D.
②“氯盐酸浸”时,通入的目的是。

①除去原料气中CO的理由是。
②为提高CO吸收率,应选择的条件为。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
③中的配体为

①该反应历程中最大活化能对应步骤的化学方程式为。合成氨反应:的
(用图中字母表示)。
②铁催化合成氨时与
需吸附在催化剂表面活性位点进行反应,由合成氨反应的速率方程
(k为速率常数)可知,
越大,反应速率越小。原因是。
①含有苯环,能使溶液显色:
②核磁共振氢谱中有6个化学环境相同的氢原子。
写出核磁共振氢谱中峰面积为6:2:1:1的同分异构体的结构简式(任写一种)。
