
B .
B . 
C .
C . 
D .
D . 
 B .
B .  C .
C .  D .
D . 
 检验氧气
B .
检验氧气
B .  检查气密性
C .
检查气密性
C .  称量氯化钠
D .
称量氯化钠
D .  给液体加热
给液体加热
| A | 空气是宝贵的资源 | B | 实验操作安全常识 |
| 氮气﹣﹣填充食品袋防变质 二氧化碳﹣﹣光合作用原料 稀有气体﹣﹣制作霓虹灯 | 不可以将鼻孔凑到容器口去闻药品气味 为获得感性认识,可触摸药品和品尝味道 停止加热时,要用嘴吹灭酒精灯 | ||
| C | 测空气中氧气含量实验成功关键 | D | 加热时试管破裂原因 |
| 装置气密性好 药品(红磷)足量 打开弹簧夹时机:装置冷却 | 加热前没有给试管预热 加热时试管外壁沾有水珠 加热后立即用冷水冲洗 |
选项 | 客观事实 | 解释 |
A | 湿衣服在阳光下比在阴凉处干得快 | 温度越高,分子运动速率越快 |
B | 温度计测量热水温度时水银柱升高 | 汞原子受热体积增大 |
C | 氧气和液氧都能支持燃烧 | 同种分子化学性质相同 |
D | 稀有气体可制成多种用途的电光源 | 稀有气体在通电时能发出不同颜色的光 |

 B .
B .  C .
C .  D .
D . 
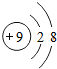 B .
B .  C .
C . 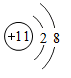 D .
D . 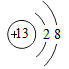

| | | | |
| A.观察到有水和二氧化碳生成 | B.蜡烛熄灭时,产生白烟是化学变化 | C.证明人呼出的气体中含有较多的二氧化碳 | D.证明人呼出的气体中含较多的二氧化碳 |
 加热一定质量的高锰酸钾固体
B .
加热一定质量的高锰酸钾固体
B .  将足量的硫粉与一定质量的氧气在密闭装置内引燃
C .
将足量的硫粉与一定质量的氧气在密闭装置内引燃
C .  向一定量的二氧化锰中加入过氧化氢溶液
D .
向一定量的二氧化锰中加入过氧化氢溶液
D .  用等质量的氯酸钾在有、无催化剂并加热的条件下制氧气
用等质量的氯酸钾在有、无催化剂并加热的条件下制氧气
①可吸入颗粒(如PM2.5)
②二氧化碳
③二氧化硫
④氮气


①从宏观角度看,物质A属于 (选填“混合物”或“纯净物”);从微观角度看,物质B是由 构成的(选填“分子”或“原子”或“离子”);
②该反应的符号表达式是 ,属于 。(填基本反应类型)

①锶元素在化学变化中锶原子容易失去电子变为阳离子,其离子符号为 。
②图2中微粒C是17号元素的原子,则x=。

我国提出2060年前实现碳中和,彰显了负责任大国的作为与担当。实现碳中和人人有责,让我们从衣食住行点滴做起, 节约能源, 低碳生活。
依据上文,回答下列问题:
“高氧空气”是指氧气含量高于普通空气的气体,可用于航天、医疗、炼钢等。在“新冠肺炎”重症患者的治疗上有一个重要环节为“高流氧呼吸”,其本质也和“富氧空气”差不多 ,化学兴趣小组欲混制“富氧空气”并开展相关探究, 进行以下实验。
实验一:制取氧气

①请写出仪器①的名称:;若选择A作为发生装置,则反应的符号表达式为 ;
②若用F装置收集氧气,发现氧气不纯,可能的原因是 ;
③若需测量收集氧气的体积,应在装置G的 (填“a”或“b”)导管口连接一个 ;
A.反应仓可能是H2O2溶液在MnO2催化下产生O2;
B.此仪器可用于医疗急救,也可用产生的氧气做燃料切割金属;
C.可根据加湿过滤仓中气泡的多少,来说明氧气排出的快慢;
D.加湿过滤仓利用氧气不易溶于水,来保持氧气的湿润。
学习了二氧化锰对过氧化氢溶液分解有催化作用的知识后,同学们对催化剂产生了兴趣,他们开展了以下探究。
实验探究一:比较催化剂种类对过氧化氢溶液分解的影响

【查阅资料】
①很多植物对过氧化氢溶液的分解有催化作用。
②压强传感器可以测量密闭体系内气体压强的变化。
【实验操作】
①在27.8℃,100.7kPa时,将具支试管的支管通过胶皮管与压强传感器连接(如图1所示)
②用量筒量取2mL3%过氧化氢溶液,倒入具支试管中并立即塞上橡胶塞,同时启动数据采集程序采集数据。更换相同质量,重复实验①和②。
③不加入植物碎末,重复实验①和②,做空白实验。
将采集到的数据用电脑进行处理,得到反应前后压强随时间变化曲线如图2。实验操作(3)的目的是 。【进行实验】
在30.2℃,压强100.5kPa时,选择上海青叶碎末用量分别为1g、2g、3g,获得数据如图3所示。
【实验结论2】由图3可知,在t秒内,上海青叶用量为 时,过氧化氢溶液分解速率最快;图中三条曲线最终将重合在一起。【拓展延伸】
某些植物、氧化铜、猪肝、二氧化锰等都可以做过氧化氢溶液分解的催化剂、除此以外,硫酸铜也可以作过氧化氢溶液分解的催化剂。
空气是宝贵的自然资源。图1、图2都是与空气有关的物质转化图。
①写出物质C、H物质的符号:C ,H ;
②请写出反应①的符号表达式 ;
③构成物质G的原子结构示意图:。
图2是以空气和其他必要的原料合成氮肥(NH4NO3)的工业流程。请按要求回答下列问题:
①步骤Ⅰ中发生的是 (填“物理”或“化学”)变化;
②写出步骤Ⅲ中发生反应的符号表达式 ;
③图3是化肥硝酸铵包装袋上的部分说明,硝酸铵应具有的性质是 (填字母)。
A.易溶于水
B.熔点高
C.受热易分解