一、选择题(本大题共15小题,每小题3分,共45分,每小题只有一个选项符合题意。请将符合题意的选项用2B铅笔填涂在答题卡相应位置。)
-
1.
(2024九上·长沙期末)
中华文明历史悠久。《天工开物》被誉为“中国17世纪的工艺百科全书”,其中记载的下列工艺涉及化学变化的是( )
A . 甘蔗榨汁
B . 棉纱织布
C . 酿制白酒
D . 楠木造船
-
A . 洁净的空气是纯净物
B . 氧气是空气中含量最多的气体
C . 稀有气体含量少,没有利用价值
D . 氮气化学性质不活泼,常用作保护气
-
A . 倾倒液体 B . 称量固体
B . 称量固体 C . 测定溶液的pH
C . 测定溶液的pH D . 稀释浓硫酸
D . 稀释浓硫酸
-
4.
(2024·宁明模拟)
认真观察实验现象是实验探究的重要环节之一。下列关于实验现象的描述,正确的是( )
A . 打开盛有浓硫酸的试剂瓶,瓶口出现白雾
B . 铁丝在氧气中能剧烈燃烧,火星四射,放出热量,生成黑色固体
C . 将二氧化碳通入到紫色石蕊溶液中,溶液变红,加热后溶液变成无色
D . 向硫酸铜溶液中加入氢氧化钠溶液后,产生白色沉淀
-
A . 酸
B . 碱
C . 单质
D . 氧化物
-
A . 气体可压缩存储于钢瓶中——分子之间有间隔
B . 花园里百花盛开,香气四溢——分子在不停运动
C . 水和过氧化氢的化学性质不同——分子的大小不同
D . 金刚石与石墨的物理性质差异很大——碳原子排列方式不同
-
7.
(2024九下·河东模拟)
2023年10月26日,搭载神舟十七号载人飞船的长征二号F遥十七运载火箭在酒泉卫星发射中心点火发射。经

催化后可将航天员呼出的

转化为

, 已知

中Fe为+3价,则Ni的化合价为( )
A . +1
B . +2
C . +3
D . +4
-
A . 都由碳、氧元素组成,能相互转化
B . 都能与水反应,都能使紫色石蕊溶液变红
C . 都具有可燃性,都可作为燃料
D . 都是温室气体,含量增多都能导致温室效应增强
-
A . 森林失火时,可将大火蔓延路线前一片树木砍掉,形成隔离带
B . 煤炉生火时,利用木材引燃煤炭,是为了降低煤炭的着火点
C . 燃着的酒精灯不慎碰倒,若洒出的酒精燃烧起来,应立刻用湿抹布扑灭
D . 木柴架空有利于促进燃烧,是因为增大了木柴与氧气的接触面积
-
A . 目前铜是世界上年产量最大的金属
B . 合金的硬度一般比组成其成分的金属硬度低
C . 钢铁表面刷油漆可以有效防止生锈
D . 铝有很好的抗腐蚀性能是因为化学性质不活泼
-
A . 泥沙
B . 食盐
C . 花生油
D . 面粉
-
A . 稀盐酸和稀硫酸都可以用来除铁锈
B . 熟石灰和氢氧化钠都可以用来改良酸性土壤
C . 用汽油、洗涤剂去除油污都属于乳化现象
D . 氯化钠和亚硝酸钠在生活中都可以做调味品
-
-
A . 催化剂的质量在化学反应前后不变,则在化学反应前后质量不变的物质一定是催化剂
B . 某物质在氧气中燃烧生成二氧化碳和水,则该物质一定含有碳、氢、氧元素
C . 中和反应生成了盐和水,所以能生成盐和水的反应一定是中和反应
D . 点燃氢气之前需要验纯,所以点燃甲烷之前也同样需要验纯
-
15.
(2024九上·长沙期末)
物质的分离提纯是化学学习的重要部分。除去下列物质中含有的杂质,所用试剂和方法均正确的是( )
选项 | 物质(括号内为杂质) | 除杂试剂和方法 |
A | 
| 加入足量的锌粉,过滤 |
B | 
| 加入适量的 溶液,过滤 溶液,过滤 |
C | 
| 加入足量水溶解,过滤,洗涤滤渣、干燥 |
D |  溶液 溶液
| 加入过量 溶液,过滤 溶液,过滤 |
A . A
B . B
C . C
D . D
二、填空题(本大题共4小题,化学方程式每个3分,其余每空2分,共20分。)
-
16.
(2024九上·长沙期末)
认真阅读下列材料,回答有关问题。
我国宣布在2060年前实现碳中和,“碳封存”与“碳转化”是实现碳中和目标的重要技术选择。2023年6月1日,我国首个海上二氧化碳封存示范工程项目成功投入使用,填补了我国海上二氧化碳封存技术的空白。该技术是将油井开采产生的油气混合物注入高碳分离器,再将分离出的二氧化碳通入压缩机加压和干燥,使其变成介于气态和液态之间的超临界状态。超临界状态二氧化碳密度高,接近液态二氧化碳;但其粘度小,流动快,流速接近气态二氧化碳。
利用二氧化碳资源开发化工原料,合成化工产品,有着广阔的前景。如二氧化碳与氨气 在一定条件下可合成一种常见的氮肥-尿素
在一定条件下可合成一种常见的氮肥-尿素 , 同时生成水。又如二氧化碳和氢气在一定条件下可合成甲醇
, 同时生成水。又如二氧化碳和氢气在一定条件下可合成甲醇 和水。在2023年浙江杭州进行的第19届亚洲运动会开幕式上就首次使用甲醇作为火炬燃料,该甲醇从生产到燃烧,消耗和产生的二氧化碳量实现完全中和。即“零增碳”。
和水。在2023年浙江杭州进行的第19届亚洲运动会开幕式上就首次使用甲醇作为火炬燃料,该甲醇从生产到燃烧,消耗和产生的二氧化碳量实现完全中和。即“零增碳”。
-
(1)
根据材料并结合事实分析,下列说法正确的是____(填序号)。
A . 超临界二氧化碳与二氧化碳都是由二氧化碳分子构成
B . 超临界二氧化碳比二氧化碳更容易燃烧
C . 利用二氧化碳和氨气合成尿素的化学方程式可表示为: D . 利用二氧化碳和氢气合成的甲醇中碳、氢、氧三种元素的质量比为1:4:1
D . 利用二氧化碳和氢气合成的甲醇中碳、氢、氧三种元素的质量比为1:4:1
-
(2)
碳中和,人人参与,低碳生活从我做起,你的低碳行动是(写一条即可)。
-
-
(1)
古人用硫粉涂在松木片顶端制得“发烛”。“发烛”燃烧时产生一种有刺激性气味的气体。请写出产生该气体的化学方程式:
-
(2)
某硫酸厂的污水中含有一定量的硫酸等物质,直接排放会污染水体也不利于周边农作物生长,于是人们将适量的熟石灰加入污水中,以中和其酸性,请用化学方程式解释:。
-
-
-
-
(2)
若a物质中混有少量b物质,最好采用(填“降温结晶”或“蒸发结晶”)的方法提纯a。
-
(3)
写出c的不饱和溶液转化成饱和溶液的一种方法:。
三、情境分析题(本大题共2个小题,化学方程式每个3分,其余每空2分,共11分。)
-
20.
(2024九上·长沙期末)
实验室有一包固体粉末,可能含有氢氧化钠、氯化钡、碳酸钠、硫酸钠中的一种或几种,华益兴趣小组的同学为证明其中的成分,设计了如下流程图,请根据所学知识,回答下列问题:

-
(1)
实验室进行操作Ⅰ、操作Ⅱ时,需要用到的玻璃仪器有烧杯、玻璃棒和。
-
-
(3)
小丹同学提出若在溶液A中先加入无色酚酞溶液,观察到溶液变红,再加入足量的氯化钙溶液,当观察到也能证明溶液A的成分。
-
21.
(2024九上·长沙期末)
阅读科普短文,回答下列问题。
石灰石是地壳中最常见的岩石之一,在石灰岩地区,地下水中溶有较多的二氧化碳气体,石灰岩在地下水的不断侵蚀下逐渐溶解,经过漫长的过程形成溶洞。坚硬的石灰石主要成分是碳酸钙,永不会使它溶解,但溶有较多二氧化碳的水可以和它慢慢发生化学反应,把它转化为可以溶解的碳酸氢钙 , 溶解在地下水中。
, 溶解在地下水中。
溶解有较多碳酸氢钙的地下水,在一定条件下会逐渐分解,重新生成碳酸钙沉积下来,同时放出二氧化碳,有的沉积在洞顶,有的沉积在洞底。日久天长洞顶的形成钟乳石,洞底的形成石笋,当钟乳石与石笋相连时就形成了石柱。石笋和钟乳石的形成周期非常长,需要上万年才能形成。
-
(1)
在石灰岩地区,地下水的pH7(填:“>”、“<”或“=”)。
-
四、实验探究题(本大题共2小题,每空2分,共18分)
-
-
-
(2)
利用上述仪器和药品可以制取氧气,你选择的药品是。
-
(3)
实验室可用检验C装置收集的某无色无味气体是否为二氧化碳。
-
23.
(2024九上·长沙期末)
自然界的钙多以碳酸钙的形式存在,如蛋壳、珍珠、贝壳和石灰石等主要成分都是碳酸钙。碳酸钙是一种重要的化工原料,工业用途甚广,华益中学化学兴趣小组围绕碳酸钙展开探究。
实验活动一:小滔同学向装有少量纯净的碳酸钙固体粉末的试管中加入一定量水,充分振荡,发现液体变浑浊。
-
(1)
【问题1】碳酸钙悬浊液的酸碱性怎样?
【实验探究1】
实验步骤 | 实验现象 | 实验结论 |
小滔同学继续向上层清液中加入几滴溶液。 | 上层清液变红 | 碳酸钙能部分溶于水,且形成的悬浊液显性。 |
-
(2)
【问题2】碳酸钙悬浊液变红的本质原因是什么呢?
【实验探究2】
小何同学用pH试纸先后测定出一定浓度的碳酸钠溶液、氯化钠溶液、氯化钙溶液、碳酸钙悬浊液的pH如下表所示。
| 碳酸钠溶液 | 氯化钠溶液 | 氯化钙溶液 | 碳酸钙悬浊液 |
pH试纸测定结果 | 11 | 7 | 7 | 10 |
从数据中分析可知,使【实验探究1】中的碳酸钙悬浊液变红的是碳酸钙中的(填 或
或 )。
)。
-
(3)
实验活动二:小英同学设计了如图所示实验装置探究鸡蛋壳固体中碳酸钙的质量分数。(设鸡蛋壳中杂质不溶于水,也不与稀盐酸反应,不考虑稀盐酸的挥发性,各种试剂均足量)

【实验步骤】
①连接装置,先检查装置的气密性;②称量 鸡蛋壳样品装入B中;③打开活塞K,从装置左侧通入一段时间空气;④称量装置D的质量为
鸡蛋壳样品装入B中;③打开活塞K,从装置左侧通入一段时间空气;④称量装置D的质量为 ;⑤关闭活塞K,打开分液漏斗的活塞,向B装置中逐滴加入稀盐酸至不再产生气泡后,关闭分液漏斗活塞;⑥再次称量D的质量为
;⑤关闭活塞K,打开分液漏斗的活塞,向B装置中逐滴加入稀盐酸至不再产生气泡后,关闭分液漏斗活塞;⑥再次称量D的质量为 。⑦计算:D装置的质量差
。⑦计算:D装置的质量差 即为生成的二氧化碳的质量,通过化学方程式计算得到样品中碳酸钙的质量,最终计算出样品中碳酸钙的质量分数。
即为生成的二氧化碳的质量,通过化学方程式计算得到样品中碳酸钙的质量,最终计算出样品中碳酸钙的质量分数。
【实验分析】
A装置的作用是。
-
(4)
没有C装置,则测定的碳酸钙的质量分数会(填“偏大”或“偏小”)。
-
(5)
老师指出小英的实验中碳酸钙的质量分数测定并不准确,请提出改进方法:。
五、计算题(本大题共1个小题,第1问2分,第2问4分,共6分)
-
24.
(2024九上·长沙期末)
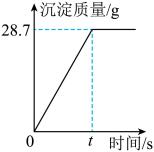
将AgNO
3溶液逐滴加入73.0g稀盐酸中,t秒后,沉淀质量不再增加,产生沉淀的质量与反应时间关系如图所示。
-
-
(2)
计算稀盐酸中溶质的质量分数(写出计算过程)。
 B . 称量固体
B . 称量固体 C . 测定溶液的pH
C . 测定溶液的pH D . 稀释浓硫酸
D . 稀释浓硫酸
在一定条件下可合成一种常见的氮肥-尿素
, 同时生成水。又如二氧化碳和氢气在一定条件下可合成甲醇
和水。在2023年浙江杭州进行的第19届亚洲运动会开幕式上就首次使用甲醇作为火炬燃料,该甲醇从生产到燃烧,消耗和产生的二氧化碳量实现完全中和。即“零增碳”。



, 溶解在地下水中。

或
)。

鸡蛋壳样品装入B中;③打开活塞K,从装置左侧通入一段时间空气;④称量装置D的质量为
;⑤关闭活塞K,打开分液漏斗的活塞,向B装置中逐滴加入稀盐酸至不再产生气泡后,关闭分液漏斗活塞;⑥再次称量D的质量为
。⑦计算:D装置的质量差
即为生成的二氧化碳的质量,通过化学方程式计算得到样品中碳酸钙的质量,最终计算出样品中碳酸钙的质量分数。
