 B . 检查气密性
B . 检查气密性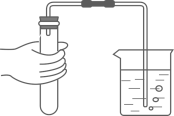 C . 点燃酒精灯
C . 点燃酒精灯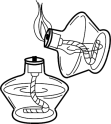 D . 倾倒液体
D . 倾倒液体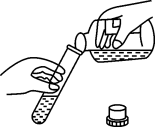

 B .
B .  C .
C .  D .
D . 
选项 | 事实 | 解释 |
A | 金刚石的硬度远大于石墨 | 碳原子排列方式不同 |
B | 干冰升华 | 二氧化碳分子的体积变大 |
C | 不同元素化学性质不同 | 元素的原子的核外电子数不同 |
D | 过氧化氢和高锰酸钾分解均能产生氧气 | 都含有氧分子 |


氯元素是一种重要的非金属元素,氯气是双原子分子构成的,常温常压下为黄绿色,密度比空气的大,能溶于水且有毒的气体。氯气可用于制备多种消毒剂、消毒泡腾片,其中二氧化氯是最新一代高效、广谱、安全环保型杀菌消毒、保鲜剂。氯气化学性质很活泼,能与水及H2等化合物反应。例如:氢气可以在氯气中燃烧生成氯化氢(HCI)气体。

①请把图1信息补充完整。横线上应填。
②氯原子在化学反应中容易(填“得到”或“失去”)电子。
在上述两个反应中,其反应物表现出还原性的是(任意写一种)。
(提示:从流程图中查找反应的条件,化学方程式一定要配平,要注明反应的条件。)

[猜想与假设]猜想Ⅰ:不相等;猜想Ⅱ:。
甲组 | 乙组 | |
实验方案 |
|
|
实验现象 | 铁钉表面有红色物质析出,溶液颜色发生改变,天平指针没有偏转 | |
结论 | 猜想Ⅰ正确 | 猜想Ⅱ正确 |
[反思评价]究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体逸出,导致指针向右偏转。得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡是有气体生成或参加的反应一定要在(填敞开容器或密闭容器)中进行。

[解释应用]解释:化学反应前后,原子的种类、数目、质量均不变,所以质量守恒。
应用:铜绿受热会发生分解反应,生成氧化铜、水和二氧化碳三种物质,则该固体物质一定由种元素组成。
加热时间/min | 0 | 10 | 20 | 30 | 40 |
固体质量/g | 14.0 | 11.6 | 9.2 | 9.2 | 9.2 |