
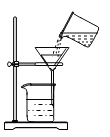
 过滤
B .
过滤
B . 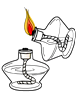 点燃酒精灯
C .
点燃酒精灯
C . 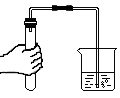 检查装置气密性
D .
检查装置气密性
D . 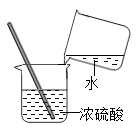 稀释浓硫酸
稀释浓硫酸

选项 | 实验目的 | 实验操作 |
A | 证明CaO能与水反应 | 加入水,测温度 |
B | 证明氧气能支持燃烧 | 伸入带火星的木条 |
C | 除去CO2气体中的CO | 通入氧气后,点燃 |
D | 除去Na2CO3中NaOH | 加入适量的稀盐酸 |


下列说法不正确的是( )


请从A或B两题中任选1个作答,若两题均作答,按A计分。
A | B |
①钠原子转化为钠离子,其核外电子数 (填“变大” 或“变小”)。 ②常温下,氯化钠饱和溶液中,氯化钠与 水的质量比为。 (已知:常温下,氯化钠的溶解度为36 g) | ①构成氯化钠的微粒是Na+和 (填微粒符号)。 ②口罩使用过程中,氯化钠溶液中溶质的质量分数(填“改变”或“不变”)。 |


i. 2H2SO3 + O2 = 2H2SO4
ii. 2Na2SO3 + O2 = 2Na2SO4
反应i、ii中化合价升高的元素是。

已知:步骤I无蓝色沉淀生成。

序号 | ① | ② | ③ | ④ |
操作 |
|
|
|
|

图1
实验 | a中试剂 | b中试剂 | c中试剂 |
I | 5%H2O2溶液 | MnO2 | 80 ℃热水 |
II | 石蕊溶液 | HCl气体 | NaOH溶液 |
已知:HCl气体极易溶解于水。白磷的着火点为40 ℃。


① 化学方程式:。
② 发生装置:。

序号 | ① | ② | ③ | ④ |
实验 |
|
|
|
|
现象 | 红色固体消失,溶液变黄 | 固体表面有气泡产生,澄清石灰水变浑浊 | ||
【资料】
i.实验室所用酚酞溶液pH<8。溶液中,酚酞的分子结构会随着pH的改变而改变,不同的结构在溶液中会表现出不同的颜色,具体如下表所示。
|
溶液的pH |
1≤pH<8 |
8≤pH≤13 |
pH>13 |
|
酚酞的分子结构 |
内酯式 |
醌式 |
羧酸式 |
|
酚酞溶液的颜色 |
无色 |
红色 |
无色 |
ii.醌式结构的酚酞能与H2O2溶液发生反应,生成无色物质,该物质在溶液中的颜色不会随着pH的改变而改变。
iii.NaOH溶液浓度越大,溶液pH越高。
该小组同学对上述资料产生了兴趣,决定对酚酞溶液颜色的变化开展探究。
【进行实验】
|
组别 |
实验操作 |
实验现象及数据 |
|
① |
1-1:配制pH为13的NaOH溶液,取5 mL于试管中,向其中滴加2滴酚酞溶液后,分成两等份 |
|
|
1-2:向一支试管中加入稀盐酸 |
溶液红色褪去 |
|
|
1-3:向另一支试管中加入 |
溶液红色褪去 |
|
|
组别 |
实验操作 |
实验现象及数据 |
|
② |
2-1:分别配制pH为8、10、11、13 的NaOH溶液,各取5 mL分别 加入4支试管中,再分别向4支 试管中加入5滴30 % H2O2溶 液,最后各滴入2滴酚酞溶液 |
每支试管中溶液都先变成红色, 然后红色逐渐褪去, 各支试管褪色时间如下图所示:
|
|
2-2:配制pH为9的NaOH溶液,分别取5 mL加入4 支试管中,再向各试管加入5滴质量分数分别为0.5%、1%、2% 、4%的H2O2溶液, 最后各滴入2滴酚酞溶液 |
每支试管中溶液都先变成红色, 然后红色逐渐褪去, 各支试管褪色时间如下图所示:
|
【解释与结论】
小组中某位同学在进行实验2-1时,滴加30 % H2O2溶液,振荡、静置30 min后,才向溶液中加入2滴酚酞溶液。静置过程中,他观察到有气泡产生;加入酚酞溶液后,他发现4支试管的褪色时间均长于原实验2-1。导致酚酞褪色时间变长的原因可能是。(忽略NaOH与空气中CO2的反应)
|
实验操作 |
实验现象 |
|
配制pH为14的NaOH溶液,取5 mL于试管中,加入5滴30 % H2O2溶液,再滴入2滴酚酞溶液 |
溶液先变红,后褪色 |
分析导致上述溶液先变红后褪色的可能原因:。