选 项 | 归 类 | 物 质 |
A | 合金 | 水银、焊锡、生铁 |
B | 氧化物 | 水、氧气、过氧化氢 |
C | 常见干燥剂 | 碱石灰、熟石灰、活性炭 |
D | 常见营养物质 | 蛋白质、维生素、葡萄糖 |
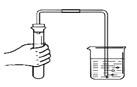 检查气密性
B .
检查气密性
B . 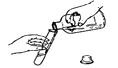 加入稀盐酸
C .
加入稀盐酸
C . 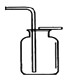 收集二氧化碳
D .
收集二氧化碳
D .  二氧化碳验满
二氧化碳验满
 B .
B .  C .
C .  D .
D . 
选项 | 物质 | 目的 | 主要实验操作 |
A | H2 (HCl)气体 | 除杂 | 先通入Na2CO3 溶液,在通过浓硫酸干燥 |
B | CaCO3、CaCl2固体 | 分离 | 溶解、过滤、洗涤、干燥、蒸发 |
C | NaOH(Na2CO3)溶液 | 检验 | 取样,滴加足量稀盐酸,观察现象 |
D | Cu、Ag | 比较活动性 | Ag片侵入CuSO4溶液中,观察现象 |
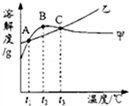
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度S/g | NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 60.2 |
| Na2SO4 | 9.6 | 20.2 | 40.8 | 48.4 | 47.5 | 47.0 | |
a.H2SO4
b.HCl
c.HNO3

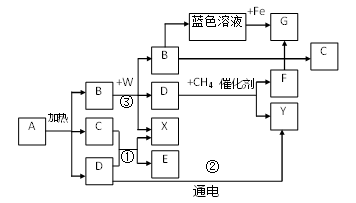
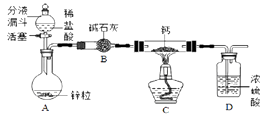
①实验室制CO2反应的化学方程式。
②装置F、H中溶液变浑浊,G中溶液不变浑浊,则原石灰水未变浑浊的原因是。
取少量上述制得的CaH2 样品加入到足量的碳酸钠溶液中,产生大量气泡,过滤,得到滤渣和滤液。经检验滤渣的成分是碳酸钙。该同学进行了如下的探究。
点燃产生的气体,火焰淡蓝色;将燃烧产物通入澄清石灰水中,无现象。则该气体为 (写化学式)。
猜想一:NaOH 猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3 猜想四:NaOH、Na2CO3、Ca(OH)2
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因
实验 | 现象 | 结论 |
实验一:取滤液,向其中滴入少量 Na2CO3溶液 |
| 猜想二不成立 |
实验二:另取滤液,向其中加入足量稀盐酸 |
| 猜想三成立 |
取制得的CaH2样品1g(杂质为未反应完的Ca)加入到足量的Na2CO3溶液中,充分反应后,过滤、洗涤、干燥称得CaCO3质量为2.4g,则该样品中CaH2的质量分数为
① 以上叙述中不涉及到的材料是(选填序号)。
A.金属材料
B.无机非金属材料
C.有机合成材料
② 我国在西汉时期就有“曾青得铁则化为铜”之说,用化学方程式表示其原理。
③ 鉴别黄铜和黄金,以下方法不可行的是(选填序号)。
A.观察颜色
B.加稀盐酸
C.在空气中灼烧
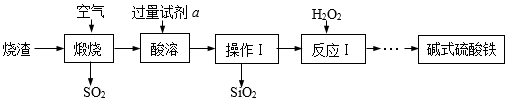
I.硫酸铜是制备其他含铜化合物的重要原料,以下是制取硫酸铜的常见方法。
方案1:向稀硫酸中加入铜粉,再用导管通入空气并加热,铜粉逐渐减少,溶液由无色变为蓝色。
①反应中溶液的pH逐渐(填“增大”或“减小”)。
②该反应的化学方程式。
兴趣小组称取此固体12.0g,在科研人员的指导下用下图装置进行热分解实验。
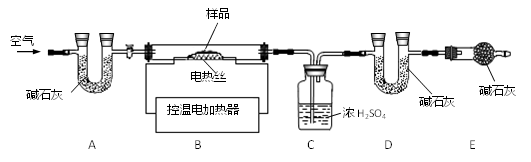
【查阅资料】Cu(OH)2的分解温度为66℃~68℃,CuCO3的分解温度为200℃~220℃,各生成对应的两种氧化物。该碱式碳酸铜失去结晶水的温度与Cu(OH)2的分解温度接近。
装置A的作用是。
|
装置 |
实验前/g |
实验后/g |
|
C |
198.0 |
199.8 |
|
D |
221.0 |
223.2 |
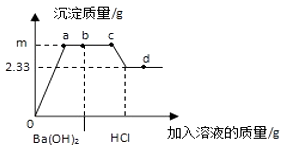
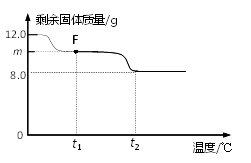
①图中F点对应的m=。
② 根据提供的数据, xCuCO3·yCu(OH)2·zH2O中x ﹕y ﹕z = 。
③ 若缺少装置E,测得的(选填“x”、“y”、“z”)的值会偏大。