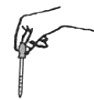
 滴加试剂
B .
滴加试剂
B . 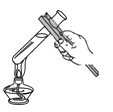 加热液体
C .
加热液体
C . 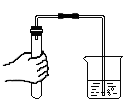 检查气密性
D .
检查气密性
D .  闻气体气味
闻气体气味
|
第1周期 |
H |
He |
||||||
|
第2周期 |
Li |
Be |
B |
C |
N |
O |
F |
Ne |
|
第3周期 |
Na |
Mg |
Al |
Si |
P |
S |
Cl |
Ar |
①Al属于(填“金属”或“非金属”)元素,其原子的核电荷数为
②Na原子的结构示意图为 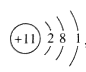 ,则钠离子的核外电子数为。
,则钠离子的核外电子数为。
③周期表中磷元素的有关信息如图所示,图中“30.97”所表示的含义是.


①写出物质X的化学式:。
②写出由物质Y转化为 的化学反应方程式:.
煤与高温水蒸气反应生成CO和 在300℃、1.5MPa、催化剂存在的条件下,CO和
可转变为液体燃料甲醇
。写出CO与
反应生成甲醇的化学方程式:。
图1 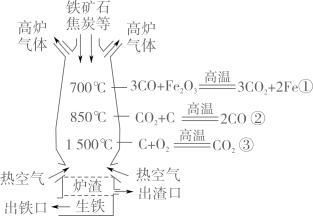
图2 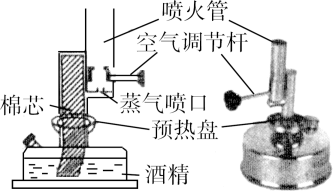
①最理想的制氢方法:在合适的催化剂作用下,利用太阳光使水分解。该制氢过程(填“吸收”或“放出”)能量,生成的氢气与氧气在相同条件下的体积之比为。
②我国稀土资源丰富,某种稀土储氢材料(用M表示)的储氢原理可表示为 。M的化学式为。
粗盐中含有不溶性泥沙、可溶性CaCl2 , MgCl2等杂质。学习小组设计了如下方案提纯粗盐:
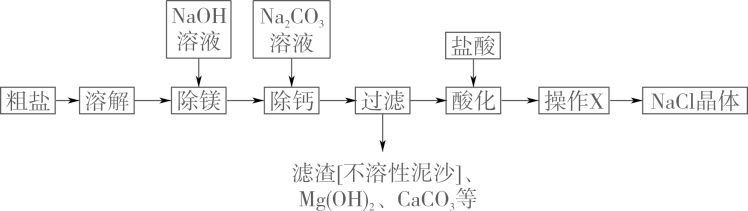
用化学方程式表示Na2CO3溶液的作用:。
步骤1:取50mL.浓氨水于锥形瓶中,加入NaCl晶体至不再溶解,制得氨盐水。
步骤2:向烧瓶中加入20mL氨盐水和约16g干冰,塞紧瓶塞,振荡、静置。一段时间后溶液中析出细小晶体,过滤、用冷水洗涤晶体并低温干燥。
(提出问题)晶体的成分是什么?
(实验探究1)①经甲同学检验,晶体中不含铵盐。甲同学的实验操作及现象是。
②乙同学取晶体少许,加入稀硝酸,晶体溶解并产生无色气体,再滴加几滴AgNO3溶液,未见明显现象,说明晶体中不含有离子。
(提出猜想)晶体的成分为Na2CO3或NaHCO3或两者的混合物。
(查阅资料)Na2CO3受热不分解;
NaHCO3受热易分解:2NaHCO3 Na2CO3+H2O+CO2↑
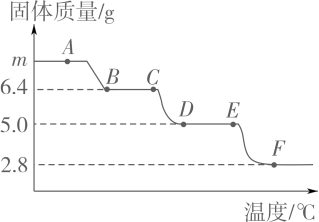
(实验探究2)称取m1g晶体,利用下图装置(夹持仪器略)探究晶体的成分。
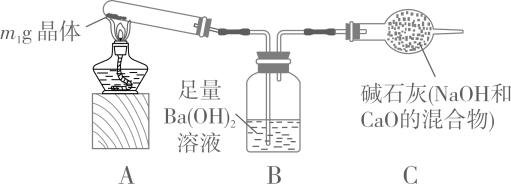
(实验现象)反应一段时间后,试管口凝结了少量小液滴,Ba(OH)2溶液变浑浊。
(实验分析)①晶体中一定含有(填化学式)。
②将晶体加热至残留固体的质量不断改变,测得残留固体的质量为m2g。
若m1g:m2g ,说明晶体为NaHCO3。
(拓展延伸)①氨盐水与二氧化碳反应所得铵盐的用途为。
②丙同学认为通过测定装置B中沉淀的质量,经计算分析也可确定晶体的组成。请对两同学的观点进行评价:。
步骤l 取100mL该葡萄酒于锥形瓶中,加入质量分数为10%的H2O2溶液,将SO2完全转化成硫酸。
步骤2 向锥形瓶中滴加指示剂(这种指示剂在pH<7的溶液中显紫色,在pH>7的溶液中显绿色),用氢氧化钠溶液中和,测得锥形瓶中硫酸的质量为14.7mg。
①步骤2中,滴入指示剂后溶液呈色。
②向10g30%的H2O2溶液中加入g水,可稀释为10%的H2O2溶液。
③通过计算判断该葡萄酒中SO2的含量是否符合国家标准。