 D .
D .  D .
D . 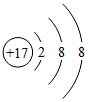


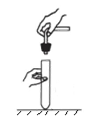 B . 贮存氧气
B . 贮存氧气  C . 过滤
C . 过滤  D . 吹灭酒精灯
D . 吹灭酒精灯 




(查阅资料)①铜锈受热易分解 ②硫酸铜粉末遇水由白色变为蓝色
(进行实验)小组同学从铜器上取下适量的干燥铜锈,按如图所示装置实验(部分夹持装置已略去)。观察到B中白色粉末变为蓝色,C中澄清石灰水变浑浊。

(解释与结论)C中反应的化学方程式是。
(提出猜想)根据铜锈的组成推测,铜生锈可能与CO2、H2O和O2有关。
(进行实验)实验小组同学取直径、长度均相同的铜丝,并打磨光亮。设计了如下图所示的5个实验并持续观察。
|
编号 |
① |
② |
③ |
④ |
⑤ |
|
实验 |
| | | | |
| 现象 | 无明显现象 | 无明显现象 | 铜丝表面 有绿色物质 | 无明显现象 | 无明显现象 |
(解释与结论)
实验中使用“经煮沸迅速冷却的蒸馏水”,其目的是。
如图所示进行实验(还测量收集的氧气体积),过氧化氢分解的化学方程式为。

|
实验序号 |
① |
② |
③ |
|
H2O2溶液的浓度% |
30 |
30 |
30 |
|
H2O2溶液的体积/mL |
6 |
6 |
6 |
|
温度/℃ |
20 |
35 |
55 |
|
MnO2的用量/g |
0 |
0 |
0 |
|
反应时间/min |
40 |
40 |
40 |
|
收集O2的体积/mL |
0 |
1.9 |
7.8 |
由此得出的结论是。
(查阅资料)H2O2溶液有一定的腐蚀性。
(进行实验)将铜片分别浸泡在以下3种溶液中进行实验,实验现象如下表:
|
编号 |
④ |
⑤ |
⑥ |
|
实验 |
| | |
| 一段时间后的现象 | 无明显变化 | 溶液变蓝,缓慢产生细小气泡 | 无明显变化 |
(解释与结论)
实验④的作用是。
小红同学提出,实验⑤中除发生(6)所给的反应外,还发生了另一个反应导致有细小的气泡产生,该反应的反应物是。
材料:1瓶(500mL)纯净水、5g蔗糖(C12H22O11)、1.5g小苏打(NaHCO3)、1.5g柠檬酸(C6H8O7)。
制备过程如下图所示:
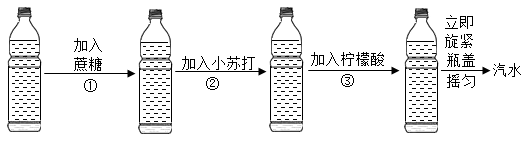
已知:小苏打与柠檬酸发生的反应为3NaHCO3 +C6H8O7=C6H5O7Na3+3H2O+3CO2↑
![]()

过程Ⅳ发生反应的化学方程式为。