材料一:1723年,施塔尔提出“燃素说”:燃素也是一种元素,燃素存在于一切可燃物中。如金属含有燃素,金属燃烧时金属释放燃素后成为金属灰(实际是金属氧化物);金属灰与燃素结合又会重新变回金属。
材料二:1766年,卡文迪许制得氢气并认为它是燃素;1773年,舍勒研究发现,可燃物燃烧需要一种他称为“火空气”的单质参与;1784年前,人们认为水是一种元素;1796年,普里斯特利制得可在“脱燃素气”中燃烧的“可燃空气”,也把它当作燃素。
材料三:1777年,拉瓦锡建立了“燃烧的氧化学说”,认为可燃物中不存在燃素;1801年,克鲁克香克证明了普里斯特利所谓的“可燃空气”是一氧化碳,从而结束了“燃素说”与“燃烧的氧化学说”之争。
|
选项 |
事实或现象 |
用“燃素说”解释 |
|
A |
金属成分比金属灰简单 |
因为金属燃烧时燃素从金属中逸出 |
|
B |
加热金属灰通入氢气,金属灰变回金属 |
因为氢气是燃素 |
|
C |
木炭与金属灰一起加热变回金属 |
因为木炭富含燃素 |
|
D |
铜在空气中加热后质量增加 |
因为金属铜中含有燃素,加热后有燃素逸出 |
|
E |
燃素(氢气)与脱燃素气(氧气)结合成为水 |
因为水是一种元素 |
取10克生石灰 粉末A质量为12克
气体B
沉淀质量为2.5克
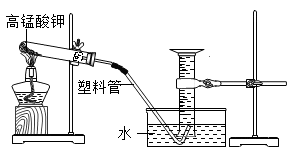



完成下列问题:
|
实验次数 |
碱面样品质量/克 |
稀盐酸质量/克 |
二氧化碳质量/克 |
|
1 |
11.0 |
50.0 |
1.1 |
|
2 |
11.0 |
200.0 |
4.4 |
|
3 |
11.0 |
250.0 |
4.4 |
|
浓度(mg/m3) |
对人体的影响 |
|
3000 |
可立即麻痹呼吸中枢, 导致瞬间死亡 |
|
120-170 |
极为危险, 会引起急性肺水肿及肺炎 |
|
40-60 |
在1小时内便可致人严重中毒 |
通过计算分析,在10米3密闭空间里,若将1.49克次氯酸钠与盐酸完全反应,产生的氯气会对人体造成怎样的影响? (次氯酸钠与盐酸反应的化学方程式为: NaClO+2HCl=NaCl+Cl2↑+H2O)