①Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物
②Na2O与CO2发生化合反应生成Na2CO3 , Na2O2与CO2发生置换反应生成O2
③Na2O是淡黄色固体,Na2O2是白色固体
④Na2O不稳定,加热能与O2反应生成Na2O2
⑤Na2O2和Na2O焰色反应均为黄色
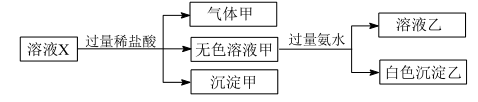
下列判断正确的是( )
①X 溶于足量水中,得到固体Y和弱碱性溶液 Z。
②取固体 Y,加足量浓盐酸,加热,产生无色气体,析出红色固体,得溶液 W。
下列结论正确的是( )
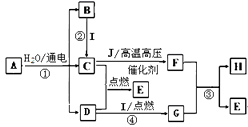
①;②; ③; ④。
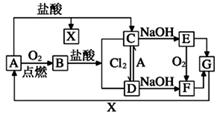

在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①该过程中涉及某氧化还原反应如下,请完成:
Fe2++□ClO-+□═□Fe(OH)3↓+□Cl-+□_
②检验滤液B中是否还含有铁元素的方法为:
③将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为(选填代号)
A.氢氧化钠溶液 B.硫酸溶液 C.氨水 D.二氧化碳
④由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、(填操作名称)、过滤、洗涤。
明矾曾经是净水明星,用离子方程式表示其净水原理。

已知:a.AlCl3·6H2O易溶于水、乙醇及乙醚;
b.铵明矾晶体无色、透明,可溶于水、不溶于乙醇。120℃时失去结晶水,280℃以上分解。
请回答:
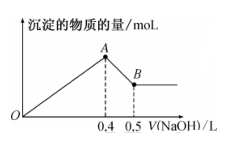
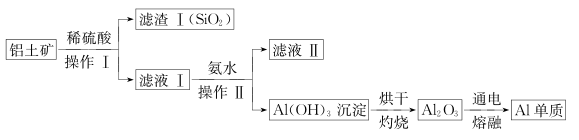 ①Al2O3与稀硫酸反应的离子方程式为 。
①Al2O3与稀硫酸反应的离子方程式为 。
②滤液II中溶质的用途之一是 。
③电解熔融的 Al2O3除得到金属铝之外,还可得到的气体产物是 (填化学式)。工业上在电解熔融的 Al2O3 时,还加入了冰晶石(Na3AlF6)作熔剂,其作用是降低 Al2O3的熔点。冰晶石在物质的分类中属于(填字母)。
a.酸 b.碱 c.盐 d.氧化物
A.Mg2+ B.Fe2+ C.Al3+ D.Cu2+
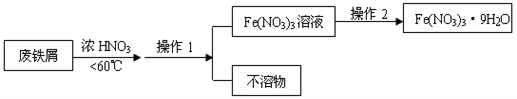
①第1步反应若温度过高,将导致硝酸分解,浓硝酸受热分解的化学方程式为。
②磁性氧化铁的化学式为,试写出Fe2O3与硝酸反应的离子方程式。
③操作1的名称为,操作2的步骤为:,过滤,洗涤。
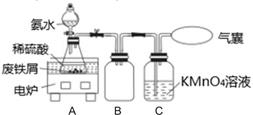
称取一定量的表面除去油污的废铁屑于锥形瓶中,加入适量的稀硫酸,在通风橱中置于50~60℃热水浴中加热充分反应。待锥形瓶中溶液冷却至室温后加入氨水,使其反应完全,制得浅绿色悬浊液。
a.保持铁屑过量
b.控制溶液呈强碱性
c.将稀硫酸改为浓硫酸
a反应生成amolN2时,转移电子的物质的量为6amol
b该反应的还原产物是硫的两种氧化物
c有amol电子转移时,生成SO2的物质的量为0.1amol
d将气体产物用足量BaCl2溶液吸收,只得到一种沉淀物
配制0.8mol/L的FeSO4溶液(pH=4.5)和0.8mol/L的(NH4)2Fe(SO4)2溶液(pH=4.0),各取2mL上述溶液于两支试管中,刚开始两种溶液都呈浅绿色,分别同时滴加2滴0.01mol/L的KSCN溶液,过了一会儿观察可见(NH4)2Fe(SO4)2溶液仍然为浅绿色透明澄清溶液,FeSO4溶液则出现淡黄色浑浊。
(资料)
|
沉淀 |
Fe(OH)2 |
Fe(OH)3 |
|
开始沉淀pH |
7.6 |
2.7 |
|
完全沉淀pH |
9.6 |
3.7 |
①请用离子方程式解释FeSO4溶液产生淡黄色浑浊的原因。
②讨论影响Fe2+稳定性的因素,小组同学提出以下3种假设:
假设1:其它条件相同时,NH4+的存在使(NH4)2Fe(SO4)2溶液中Fe2+稳定性较好。
假设2:其它条件相同时,在一定pH范围内,溶液pH越小Fe2+稳定性越好。
假设3:。