


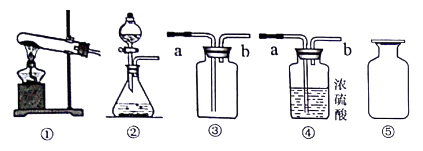
| | | | |
| A、制CO2的药品 | B、发生装置 | C、收集装置 | D、比较CO2与空气的密度 |

|
A/g |
B/g |
C/g |
|
|
甲 |
7 |
3 |
9 |
|
乙 |
6 |
4 |
9 |
|
丙 |
X |
Y |
6 |
|
丁 |
5 |
5 |
Z |

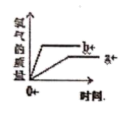 B .
B .  C .
C . 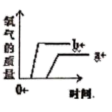 D .
D . 
 B . 贮存氧气
B . 贮存氧气  C . 过滤
C . 过滤 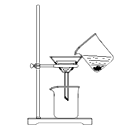 D . 吹灭酒精灯
D . 吹灭酒精灯 







通过学习资料卡片的知识,回答下列问题:
①氨气的化学性质。
②制取氨气时的发生装置应选择(填字母序号),收集裝置应选择(填字母序号)。
③氨气遇到浓盐酸冒白烟时发生反应的化学方程式。

|
实验步骤 |
实验现象 |
实验分析 |
|
①缓缓通入CO2 , 点燃甲处酒精喷灯,加热一段时间 |
木炭粉减少,丁中有气泡产生、石灰水变浑浊且。 |
硬质玻璃管中发生反应的化学方程式为,丁中现象说明。 |
|
②点燃乙处酒精灯,加热一段时间 |
乙处玻璃管内. |
乙处现象说明,反应的化学方程式为. |
|
③停止通入二氧化碳,熄灭甲、乙处的酒精灯 |
丙中有丁中液体进入 |
丙的作用是。 |

(提出问题)上述酸和碳酸盐的反应是否适合在实验室制取CO2?
(方案设计)大家经过讨论,一致认为浓盐酸不适合用于实验室制取CO2 , 你认为原因是a:;

(实验与结论)
| 实验 | 实验现象 | 实验内容 |
| A | 剧烈反应,迅速放出大量气泡 | 反应速率过快,气体不便收集,不宜于实验室制取二氧化碳 |
| B | 产生气泡,速率迅速减慢,反应几乎停止。 | 无法持续产生CO2 , 不能用于实验室制取CO2 |
| C | 产生气泡,速率适中 | 速率适中持续产生CO2 , 能用于实验室制取CO2 |
根据探究结论,实验室制取二氧化碳选择第C组药品,该药品制取二氧化碳的反应原理是b:用化学方程式表示为c:;验满方法是d:;检验方法是e:。

现象:第一朵紫色干花喷上水,紫花不变色;第二朵紫色干花直接放入盛满二氧化碳的集气瓶中,紫花也不变色;第三朵紫色干花先喷上水,再放入盛二氧化碳的集气瓶中,紫花(填写关于颜色的现象)。结论:以上实验现象说明:。反应的化学方程式是:。
①所选仪器的连接顺序为:(填写仪器序号字母),点燃氢气前,先要检验氢气的;以免氢气发生爆炸。氢气燃烧的方程式是:。
②生成氢气时,所发生反应的化学反应方程式。
①仪器B的作用是;
②仪器A中生成氧气的化学方程式是:;
③欲通过测量反应前、后C处大玻璃管质量的增加,来计算样品中CuO含量。若反应后大玻璃管中红色的Cu还没有完全消失,则样品中CuO含量的测算结果将(填“偏大”“偏小”“不受影响”)。
写出图中标号仪器的名称:①。
用以下三种方法收集二氧化碳,并用装置C测定集气瓶内气压。每种方法均做三次实验,取平均值,实验数据记录在下表中。
方法1、当装置B开始产生气泡15s后,用排水法收集气体,记录集满二氧化碳气体所用的时间为t。
方法2、当装置B开始产生气泡15s后,用向上排空气法收集,收集时间采用方法一所用的平均时间t0。
方法3、当装置B开始产生气泡15s后,用向上排空气法收集,同时用燃着的木条放在集气瓶口,待木条熄灭,立即盖上玻璃片。
|
方法1 |
方法2 |
方法3 |
|
|
瓶内初始气压(kPa) |
104.2 |
104.2 |
104.2 |
|
三次实验最终气压平均值(kPa) |
9.3 |
31.8 |
39.7 |
|
CO2纯度 |
91.1% |
69.5% |
X |
三种方法均在15s后开始收集的原因是。
在光催化条件下,CO2和H2反应生成甲烷(CH4)和水,反应的化学方程式为。
|
1 |
甲 |
乙 |
丙 |
丁 |
|
大理石 |
m克,块状 |
m克,块状 |
m克,粉末状 |
m克,粉末状 |
|
盐酸(过量) |
w克,稀盐酸 |
w克,浓盐酸 |
w克,稀盐酸 |
w克,浓盐酸 |

提出问题:用山泉水配制的氢氧化钠溶液为什么会出现浑浊,白色沉淀是什么物质?
作出猜想:Ⅰ、氢氧化钠样品不纯,含不溶性杂质;
Ⅱ、氢氧化钠与溶解在山泉水中的某物质发生反应生成难溶于水的物质。
|
主要操作 |
实验现象 |
解释或化学方程式 |
|
取少量的沉淀物,加入适量稀盐酸 |
|
沉淀物中含碳酸钙。该反应的化学方程式是 |