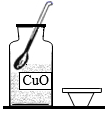
 取用药品
B .
取用药品
B . 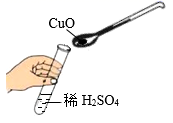 添加药品
C .
添加药品
C . 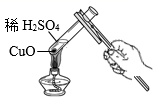 加快反应
D .
加快反应
D . 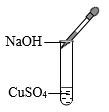 滴加碱液
滴加碱液


①鼓入足量空气能使木炭从而提高炉温。
②炼锡时,有关键的一步“点铅勾锡”,即加铅能使锡较易熔化流出,其原因是。
①锡往往与其它金属制成合金使用,目的是(选填 “增大”或“减小”)硬度。
②古代锡器常用来饮酒喝茶,很少装酸性物质,原因是。

①向其中一套锥形瓶内加入30mL水,搅一段时间后打开止水夹,观察到轻质塑料球向左移动一小段,移动原因是,实验中b管的作用为:平衡气压有利于液体顺利滴下和。
②向另一套装置的锥形瓶内加入30mL6%的NaOH溶液,搅排一段时间后打开止水夹,观察到轻质塑料球向左移动的距离比①中大得多,主要原因可用化学方程式表示为,随后,向锥形瓶内加入足量稀盐酸搅拌,可观察到轻质型料球(选填向左”、“向右”或“不”)移动。

再关闭止水夹,拔下注射器。
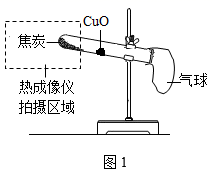
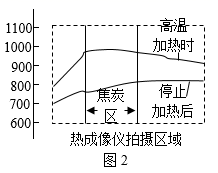
①将CuO加水制成糊状,用毛笔刷在试管内壁,烘干;然后在试管底部加入一定量的焦炭,再向试管里通入干燥的CO2 , 此时用仪器测得CO2含量为ag/L,用气球密封试管口。
②用酒精灯加热试管中的氧化铜部位一段时间,无明显现象,随后熄灭酒精灯。
③高温加热焦炭部位一段时间,停止加热,用热成像仪拍摄图1中虚线框部位,数据输出得到图11。恢复至与①相同的条件测得CO2含量为0.2ag/L。
④再次用酒精灯加热氧化铜部位,1分钟左右黑色固体变成紫红色。
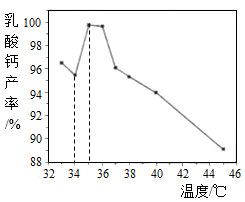


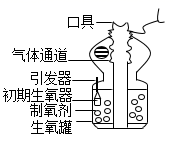
(查阅资料1)
①该化学氧自数器在工作初期,内部独立的“初期生氧器”首先启动,以解决初期供氧不足的问题。“初期生氧器”内有氯酸钾、二氧化锰、铁粉等成分。
②Fe3O4能与硫酸反应,其化学反应方程式为:Fe3O4+4H2SO4 =Fe2(SO4)3+FeSO4+4H2O
“初期生氧器”主要依靠氯酸钾和二氧化锰制氧,其化学反应方程式为。
(实验探究1)
|
序号 |
实验步骤 |
实验现象 |
实验结论 |
|
① |
取“初生氧器”充分反应后的物质于纸上,将磁铁靠近并接触粉末 |
有黑色物质被磁铁吸引 |
被吸引物质可能是Fe、Fe3O4或两者都有 |
|
② |
取①中被铁吸引的物质于试管中,向其中加入足量稀硫酸 |
固体完全溶解,得到澄清的黄色溶液 |
被吸引物质中一定含有(填化学式) |
(查阅资料2)
①该化学氧自救器主体是由“生氧罐”供氧,内部装有颗粒状超氧化钾作为“制氧剂”,其反应原理为:4KO2+2H2O=4KOH+3O2↑;4KO2+2CO2=2K2CO3+3O2
②超氧化钾能与硫酸反应,其化学反应方程式为:4KO2+2H2SO4 =2K2SO4+3O2↑+2H2O
(实验探究2)
同学们对超氧化钾是否变质展开了研究,取出久置的“生氧罐”内颗粒状固体,称得样品质量为69.3g,进行如图所示实验,待实验结束测得C装置增重2.2g,E装置内固体变黒色且增重19.2g(实验前已排尽装置内空气,使用的药品均足量)

反应开始后A装置中通入N2的目的是。