 表示向硫酸铜溶液中不断滴入氢氧化钡溶液
B .
表示向硫酸铜溶液中不断滴入氢氧化钡溶液
B .  表示将两份质量相等的固体物质分别加热制取氧气
C .
表示将两份质量相等的固体物质分别加热制取氧气
C .  表示向一定温度下氢氧化钙的饱和溶液中加入少量氧化钙固体
D .
表示向一定温度下氢氧化钙的饱和溶液中加入少量氧化钙固体
D .  表示向等质量的镁条和铝条中分别加入足量的溶质质量分数相同的稀硫酸
表示向等质量的镁条和铝条中分别加入足量的溶质质量分数相同的稀硫酸
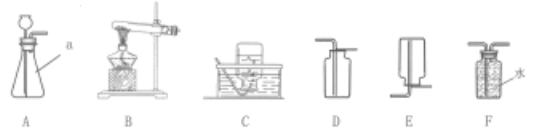
 B . 检查气密性
B . 检查气密性 C . 加热固体
C . 加热固体 D . 氧气验满
D . 氧气验满



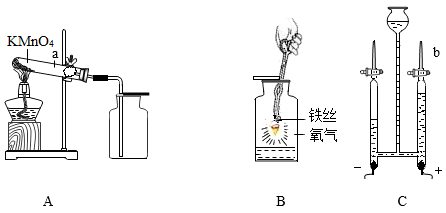
①图中用于加热试管的仪器名称是。
②诺将装置A和E连接制取气体X,A中反应的化学方程式为。
③诺用装置B和F制取气体X,装置中a和c相连,则气体X是。
【操究活动1】①将一定量的过氧化钙加入水中,缓慢产生气泡(经检验该气体能使带火星的木条复燃);
②取少量反应后的液体于试管中,滴加酚酞试液,溶液变红。据此得出反应的化学方程式为。
【探究活动2】另取①中上层清液,加入Na2CO3溶液,充分反应后有沉淀生成,生成沉淀的化学方程式为。过滤,得到滤渣和滤液。
【作出猜想】猜想一:NaOH 猜想二: 猜想三:NaOH、Na2CO3

查阅图1,动植物呼吸(填“能”或“不能”)释放CO2。
自然吸收:查阅图1,CO2的自然吸收途径有(填图中序号)。

①反应、分离室中发生复分解反应的化学方程式为。
②流程中可循环利用的物质有CaO、。
我国科学家在实验室实现以CO2和H2为原料人工合成淀粉(C6H10O5)n , 若用44gCO2人工合成淀粉(假设反应过程中无含碳物质的加入和损失),理论上制得淀粉的质量为g。

①
②
③
结合以上装置,适合作为实验室制取NH3的反应原理有(填序号)。
小吴按照说明书将适量茶垢清洁剂放入有茶垢的杯子中,加入热水浸没茶垢,立即产生大量气泡,一段时间后冲洗茶杯,茶杯光亮如新。
【查阅资料】茶垢清洁剂的主要成分为过碳酸钠(Na2CO4)。
【猜想与假设】同学们对该气体的成分提出了三种猜想。
猜想1:只有O2;猜想2:;猜想3:既有O2又有CO2。
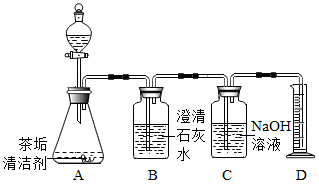
操作 | 现象 | 结论 |
检查气密性后,向A中加入热水,将生成的气体依次通过B、C,向D中插入带火星的木条。 | 观察到B中,D中木条复燃。 | 猜想1正确。 |
【猜想与假设】同学们查阅资料后,作出三种猜想。
猜想1:只有Na2CO3;
猜想2:只有NaOH;
猜想3:既有Na2CO3又有NaOH。
【实验验证】小施从下列试剂中选择合适的试剂完成探究:稀盐酸、饱和Ca(OH)2溶液、CaCl2溶液、酚酞溶液、Ba(OH)2溶液。
操作 | 现象 | 结论 |
步骤1:取少量溶液E,滴加。 | 有气泡产生 | 溶液中一定有 Na2CO3 , 猜想2不正确。 |
步骤2:另取少量溶液E,滴加CaCl2溶液至不再产生沉淀为止,向上层清液中加入。 | 无明显现象 | 溶液中无NaOH,猜想3不正确,猜想1正确。 |
①根据过碳酸钠的性质,保存茶垢清洁剂应注意。
②过氧化钠(Na2O2)常用作供氧剂,其与水反应的历程与过碳酸钠类似,即先与水反应生成过氧化氢和一种碱,之后过氧化氢迅速分解。请写出过氧化钠与水反应的总反应方程式。

①用装置A制取氧气,反应的化学方程式为。用装置E收集氧气,检验是否集满的方法是(写出操作、现象和结论)。
②用过氧化氢溶液和MnO2混合制取氧气,反应后通过、洗涤、干燥等操作回收MnO2。
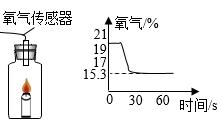
①可燃物燃烧的条件之一是。
②当氧气浓度变为%时蜡烛不再燃烧。
③蜡烛熄灭后集气瓶中含量最多的气体是。
评价标准 |
①是否根据实验条件选择实验方案,并进行可行性论证 |
②是否积极参与实验操作活动,并善于与同学合作 |
③是否规范取用药品,节约药品,保持实验台整洁 |
④是否客观准确记录实验现象,并交流实验成果 |
⑤是否体验到实验探究活动的乐趣 |
你是某小组成员,参与完成下列实验活动。
你所选方案对应反应的化学方程式为。
小组讨论决定选用A方案。
①同学甲负责选择组装制取气体装置的仪器。她选择了铁架台、带有导管的橡胶塞、水槽、试管,还应根据下图所提供的仪器,选择、(填仪器名称)。

②同学乙负责取用药品。他先检查装置气密性,再用纸槽小心地把高锰酸钾粉末送至试管(填“中部”或“底部”)后直立试管,抽出纸槽。
③同学丙负责组装仪器。他按“从下到上、从左到右”的顺序组装制取装置,固定试管时注意到试管口应略。
④你负责排水法收集氧气。开始收集的时机是。收集到两瓶气体,均呈红色。
⑤实验结束,待试管冷却,将残余物倒入指定容器,用(填仪器名称)洗涤试管;整理实验台,报告老师后离开实验室。

装置B中仪器甲的名称是。

“管道疏通剂”包装袋上相关信息如图。
查阅资料:铝和氢氧化钠固体遇水反应放出大量的热,能加快氢氧化钠对毛发等淤积物的腐蚀,同时产生的气体能增加管道内的气压,利于疏通。该反应的化学方程式为:。(注:NaAlO2名称为偏铝酸钠,溶液显碱性,)
小夏取少量该疏通剂加入适量水,充分反应后,无固体残留,说明疏通剂中一定已完全反应。取少量反应后溶液,向其中滴入1滴酚酞试液,可观察到溶液呈色。
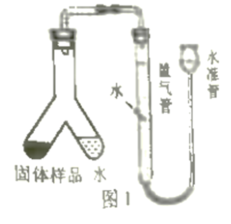
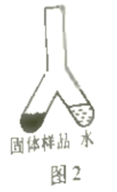
小文设计了图1装置测定该疏通剂样品中铝粉的质量分数。将300mg固体样品和足量水分别放在Y形管两侧,倾斜Y形管,将水倒入左侧:充分反应后,冷却到室温,利用量气管和水准管测定反应生成的氢气体积为100mL。已知该条件下氢气密度为0.09mg/mL。请计算样品中铝粉的质量分数。(写出计算过程)。


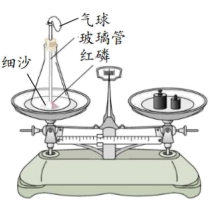
①用红热的玻璃管引燃红磷,其燃烧过程中能观察到的现象是,反应的化学方程式为。
②待红磷熄灭后再次称量,天平不再平衡,其原因可能是。
A.装置漏气
B.用橡胶塞塞紧锥形瓶速度太慢
C.红磷太少
D.没有等锥形瓶冷却就再次称量
步骤1:在锥形瓶中加入适量的CuSO4溶液,塞好橡胶塞。将几根铁钉用砂纸打磨干净,将盛有CuSO4溶液的锥形瓶和铁钉一起放在托盘天平上称量,记录所称质量为m1。
步骤2:将铁钉浸入到CuSO4溶液中,塞好橡胶塞。观察实验现象,待反应有明显现象后,将盛有CuSO4溶液和铁钉的锥形瓶一起放在托盘天平上称量,记录所称质量为m2
①用砂纸将铁钉打磨干净的作用是。
②步骤2中可观察到明显的实验现象是。该变化可说明Fe和Cu的金属活动性由强到弱的顺序是。
③若m1=m2 , 可证明参加反应的Fe和CuSO4的质量总和等于。
①若要证明CuSO4溶液对H2O2分解具有催化作用,除需证明CuSO4在反应前后化学性质和质量不发生改变外,还需证明的是。
②为探究CuSO4在反应前后质量是否发生改变,某同学设计如下实验:
向H2O2溶液中滴入10ga%的CuSO4溶液,待反应完全后,向试管中加入足量的BaCl2溶液,产生沉淀,过滤、洗涤、干燥,称量沉淀物为bg。
上述实验步骤中若缺少“洗涤、干燥”,则通过沉淀物bg计算出溶液中CuSO4的质量0.1ag。(填“大于”或“小于”或“等于”)

①650℃时,CuSO4开始发生分解反应,生成CuO和另一种氧化物X,X的化学式为。
②1000℃时,CuO开始发生分解反应,生成Cu2O和O2.计算图中m的值。(写出计算过程)
实验步骤 | 实验现象 | 实验结论 |
| 步骤①木条不复燃; 步骤②产生气泡,溶液变蓝色; 步骤③。 | 硫酸铜能作过氧化氢分解的催化剂,反应的化学方程式为。 |
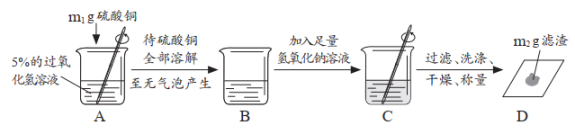
根据上述实验中m1:m2=,证明反应前后铜离子没有发生变化;将实验方案中的氢氧化钠溶液换成溶液,再次实验,证明反应前后硫酸根离子也没有发生变化。