 B .
B .  C .
C . 

 B .
B .  C .
C .  D .
D . 
A.测量空气中氧气含量偏低的原因 | B.化学中的“先”与“后” |
①红磷的量不足 ②没有冷却到室温就打开止水夹 ③燃烧匙伸入集气瓶中的速度太慢 | ①点燃可燃性气体,先验纯后点燃 ②给试管里的药品加热,先预热后固定加热 ③用一氧化碳还原氧化铁,先加热后通入一氧化碳 |
C物质的除杂(括号内为杂质) | D.物质的鉴别 |
①CO2(CO):点燃 ②Cu(Fe):放入过量稀硫酸,过滤 ③FeCl2(CuCl2):放入过量铁粉,过滤 | ①CO和CO2一一澄清石灰水 ②N2和O2一一带火星的木条 ③黄铜和黄金一一用火烧 |
 通电电解水
B .
通电电解水
B . 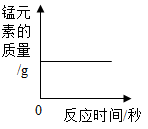 加热一定质量的高锰酸钾
C .
加热一定质量的高锰酸钾
C .  向等质量的铁、锌中分别加入足量的等浓度的稀盐酸
D .
向等质量的铁、锌中分别加入足量的等浓度的稀盐酸
D .  用等质量、等浓度的过氧化氢溶液分别在有、无催化剂的条件下制氧气
用等质量、等浓度的过氧化氢溶液分别在有、无催化剂的条件下制氧气
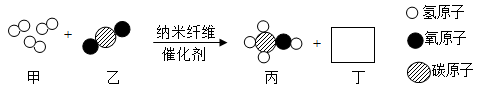

①铁丝生锈的同时发现试管中水面上升,其原因是。
②铁丝生锈的条件是。
③校园里篮球架可采取的防锈措施是什么?。


①D→A:。
②C→E:。

①实验室制氧气
②实验室制氢气
③实验室制二氧化碳
④利用无水醋酸钠和碱石灰两种固体共热制甲烷


【猜想与假设】小明依据生活中常见金属的种类,提出如下猜想:①铝;②铁;③锌;④锡;⑤铜,小组同学讨论后认为猜想⑤不成立,理由是。
【进行实验】
实验1:取一块完整的“锡纸”,反复折叠,观察到。据此得出猜想③不成立
实验2:小红利用物理性质设计了一个简单实验,很快证明了猜想②不成立。她的实验操作及现象是。
方案1:向试管甲中加入一定量稀盐酸,依据反应速率快慢进行判断。
方案2:向试管乙中加入一定量硫酸锌溶液,依据是否产生新金属进行判断。小组同学讨论认为小刚的两种方案都不合理。他们的理由如下:
方案1 | 实验中只有“锡纸”所用的一种金属,无法进行反应速率的比较:金属与酸的反应速率除与金属活动性有关外,还与(写一种即可)有关。 |
方案2 | 由于,锡和硫酸锌溶液不反应,实验中观察不到明显现象;铝与硫酸锌溶液反应,其反应的化学方程式为,但反应生成的新金属与铝的颜色相同,现象也不明显,故难以短时间内进行准确判断。 |
实验4:在老师的建议下,小组同学决定通过称量“锡纸”与硫酸锌溶液反应前后固体的质量进行探究。反应前已处理的“锡纸”质量为m,与硫酸锌溶液反应后所得固体(已进行必要的洗涤和干燥)质量为n。小组同学依据(选填“m=n”“m<n”或“n”),并查阅相关资料,最终得出猜想①成立。
【拓展延伸】由于锡的熔点低,160℃以上时就会发生脆化,所以限制了锡纸的应用,现代工艺中用铝代替锡做成“锡纸”。
|
反应前 |
反应后 |
|
|
烧杯和稀盐酸总质量 |
鸡蛋壳的质量 |
烧杯和剩余物总质量 |
|
150g |
6.25g |
154.05g |