 测定溶液的pH
B .
测定溶液的pH
B .  称量固体
C .
称量固体
C .  检查气密性
D .
检查气密性
D .  过滤悬浊液
过滤悬浊液
| 液体 | 胃液 | 胰液 | 胆汁 | 血浆 |
| pH | 0.9-1.5 | 7.5-8.0 | 7.1-7.3 | 7.35-7.45 |
下列液体中,碱性最强的是( )

 B . 加热液体
B . 加热液体 C . 测定某溶液的pH
C . 测定某溶液的pH D . 检查气密性
D . 检查气密性
 B . 小气球变大
B . 小气球变大
 C . 验证Fe、Cu、Ag金属活动性强弱
C . 验证Fe、Cu、Ag金属活动性强弱
 D . U型管内液面左高右低
D . U型管内液面左高右低


①图甲,向质量和质量分数都相等的稀盐酸中分别加入足量的锌粉和铁粉
②图乙,向一定量的氢氧化钠溶液中加水稀释,溶液的pH变化
③图丙,向一定量的稀盐酸和氯化铜的混合溶液中不断滴加氢氧化钠溶液
④图丁,在一定量Fe(NO3)2、AgNO3和Cu(NO3)2的混合溶液中加入铁粉
 向二氧化锰中加入一定量的双氧水
B .
向二氧化锰中加入一定量的双氧水
B .  向一定量的稀盐酸中加入氢氧化钠溶液至过量
C .
向一定量的稀盐酸中加入氢氧化钠溶液至过量
C .  向盐酸和氯化钙的混合溶液中逐滴加入纯碱溶液至过量
D .
向盐酸和氯化钙的混合溶液中逐滴加入纯碱溶液至过量
D .  向等质量的镁粉和铝粉中分别加入过量等质量分数的稀硫酸
向等质量的镁粉和铝粉中分别加入过量等质量分数的稀硫酸
①Zn+ H2SO4=ZnSO4+H2↑ ②ZnO+H2SO4=ZnSO4+H2O
③Zn(OH)2+H2SO4=ZnSO4+2H2O ④ZnCO3+H2SO4=ZnSO4+ H2O+CO2↑
对这四个化学反应,错误的是( )

 B .
B .  C .
C .  D .
D . 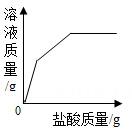

| x | y | |
| A | NaOH溶液 | 稀HCl(过量) |
| B | 稀H2SO4 | BaCl2溶液(少量) |
| C | Ca(OH)2 | CO2(适量) |
| D | 稀NaOH | H2O |
 B . 倾倒液体
B . 倾倒液体  C . 稀释浓硫酸
C . 稀释浓硫酸  D . 取用块状固体
D . 取用块状固体 
| 选项 | 物质 | 目的 | 主要实验操作 |
| A | Fe 粉末和 CuO 粉末 | 鉴别 | 取样,分别滴加稀 H2SO4 ,观察现象 |
| B | 稀硝酸中含有稀盐酸 | 验证 | 取样,加入适量硝酸银溶液,观察现象 |
| C | 硫酸铁溶液中混有少量硫酸 | 除杂 | 加入足量的铁粉,过滤 |
| D | CaCl2 和 CaCO3 固体混合物 | 分离 | 加水溶解、过滤, 洗涤干燥滤渣, 并蒸发滤液 |


A.KOH
B.Na2CO3
C.草木灰(主要成分K2CO3)
D.NH4Cl
A.熟石灰B.食盐C.浓硫酸D.干冰E.稀盐酸



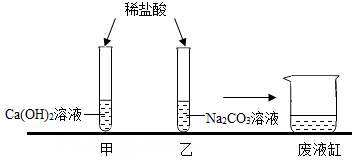
实验现象:一段时间后,看到气泡从植物表面冒出,导管①的管口处有水排出,溶液呈绿色。将带火星的木条放在导管②的管口处,打开K2 , 木条复燃。
实验结论:。
猜想一:只含有NaOH 猜想二:含有NaOH、Na2CO3
猜想三:含有NaOH、Ca(OH)2 猜想四:含有NaOH、Ca(OH)2、Na2CO3
讨论后,大家一致认为有一个猜想是错误的,请指出错误的猜想并说明理由(用化学方程式表示理由)。
|
实验操作 |
实验现象 |
结论 |
|
在试管甲中继续滴加碳酸钠溶液 |
猜想三错误 |
|
|
在试管乙中滴加足量稀盐酸 |
开始无明显现象,后产生气泡 |
猜想二正确 |

猜想1:没有发生复分解反应,溶液中有MgCl2 , 即Mg2+和Cl-同时存在溶液中。
猜想2:试管②中发生了复分解反应,溶液中无MgCl2。
老师提示SO42-会对Cl-的检验有干扰,需要先除去,小明根据老师的提示和自己的猜想提出了以下实验方案。
[设计方案]
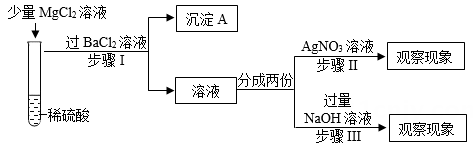
|
实验次数 |
1 |
2 |
3 |
4 |
5 |
|
稀硫酸的用量/克 |
20 |
20 |
20 |
20 |
20 |
|
剩余固体的质量/克 |
17.4 |
14.8 |
12.2 |
12.0 |
12.0 |
分析数据,回答下列问题:

| 实验次数 |
第1次 |
第2次 |
第3次 |
第5次 |
| 稀盐酸用量/克 |
5 |
5 |
5 |
5 |
| 剩余固体质量/克 |
3 |
2 |
1 |
1 |

