
查阅资料:①碱石灰由CaO和NaOH固体混合而成,常用于吸收CO2和干燥气体。
②Ba(NO3)2溶液呈中性。
提出猜想:该碱石灰的主要成分可能含有CaO、NaOH、Ca(OH)2、CaCO3和Na2CO3。
步骤Ⅰ.取部分该碱石灰样品于试管中加足量水,没有明显放热现象,充分振荡并静置后有白色沉淀,将上层清液分别倒入试管A、B、C中。
步骤Ⅱ.向试管A中滴加稀盐酸,有气泡产生。
步骤Ⅲ.向试管B中滴加酚酞,溶液变红色,说明滤液呈。
步骤Ⅳ.向试管C中加入过量Ba(NO3)2溶液,有白色沉淀生成。静置后向上层清液中滴加酚酞,溶液不变色。
实验结论:该碱石灰样品中含有的物质是 。

氧化物的有。


请完成下列分类表中相关内容
|
分类的标准 |
物质类别 |
|
|
类别一 |
O2 S Fe Cu |
|
|
类别二 |
CO2 H2O |
|
|
类别一 |
O2 CO2 H2O |
|
|
类别二 |
S Fe Cu |
|

|
组合 |
| | | |
| 现象 | 铜片表面产生气泡, 锌表面没有气泡 | 银片表面产生气泡, 锌表面没有气泡 | B片表面产生气泡, A片表面没有气泡 | C片表面产生气泡, B片表面没有气泡 |

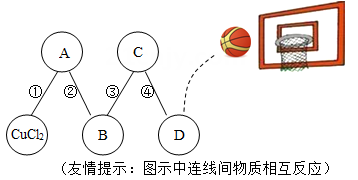

① 若溶液 C 中只含一种溶质,则样品中没有。
② 通过测氢气的质量,也可确定样品的成分,则 w 的值为(用 m 和 n 的代数式表示)。
①取适量粉末溶于水中,形成无色澄清溶液,杯底无沉淀物。
②取适量步骤①所得溶液,用吸管向其中吹“泡泡”。过一会儿, 溶液出现浑浊现象:
③另取步骤①所得溶液,滴加硝酸银溶液,产生白色沉淀。
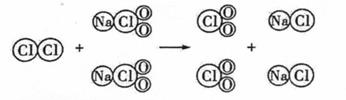
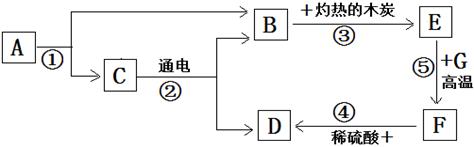

根据以上信息回答下列问题:

Ⅰ.取样于烧杯中,加足量水充分溶解,过滤得到白色沉淀物甲和滤液A;
Ⅱ.往滤液A中加入一定量的呈中性的氯化钡溶液,充分反应后并过滤。得到白色沉淀物乙和滤液B;
Ⅲ.往滤液B中滴加酚酞试液,发现溶液呈红色;
Ⅳ.取白色沉淀物乙,加入足量的稀硝酸,发现有无色气体产生且沉淀全部消失。
请回答下列问题:
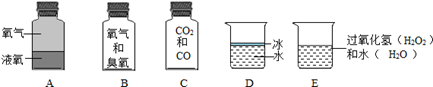

①CH4+H2O CO+3H2
②2CH4+O2 2CO+4H2
从原料配比角度比较方法①和②,更适宜用于合成甲醇的方法是(填序号)。