

|
选项 |
实验 |
现象 |
结论 |
|
A |
向某溶液中滴加氯水,再滴加KSCN溶液 |
溶液变成红色 |
该该溶液中一定含有Fe2+ |
|
B |
取少量铁与水蒸气反应后的固体,先加入稀盐酸再加KSCN溶液 |
溶液呈浅绿色 |
样品中没有+3价铁 |
|
C |
向蛋白质溶液中加入CuCl2或 |
均有沉淀 |
蛋白质均发生了变性 |
|
D |
向0.1mol/LMgSO4溶液缓慢滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol/LCuSO4溶液 |
白色沉淀逐渐变为蓝色沉淀 |
|
实验 | 实验操作和现象 |
1 | 把SO2通入氨水,测得溶液pH=7 |
2 | 向0.1mol/LNa2SO3溶液中加入过量0.2mol/LCaCl2溶液,产生白色沉淀 |
3 | 向0.1mol/LNaHSO3溶液中滴入一定量NaOH溶液至pH=7 |
4 | 把少量氯气通入Na2SO3溶液中,测得pH变小 |
下列说法错误的是( )

目的 | 方案设计 | 现象和结论 | |
A | 验证NaCl、Na2SO4、NaOH混合溶液中的Cl- | 取混合溶液于试管中,加入过量的Ba(NO3)2溶液充分反应,静置,向上清液中滴加AgNO3溶液 | 若上清液变浑浊。则混合溶液中含有Cl- |
B | 证明氧化性:Cl2>Fe3+> | 向2支盛有FeCl2溶液的试管中分别加入氯水。向其中一支滴加KSCN溶液,向另一支依次滴加H2SO3溶液相BaCl2溶液 | 第一支试管中溶液变成血红色, 第二支试管中产生白色沉淀,则证明氧化性:Cl2>Fe3+> |
C | 证明CH4和Cl2光照下发生取代反应 | 将装有干燥Cl2的集气瓶倒扣在装有干燥CH4的集气瓶上,抽出玻璃片,置于光照条件下反应 | 观察到集气瓶内出现白雾,则证明CH4与Cl2发生了取代反应 |
D | 探究AgCl和AgI的溶解度的大小 | 向2支盛有2mL相同浓度硝酸银溶液的试管中分别加入相同滴数同浓度的NaCl和NaI溶液 | 若一支试管中无明显现象,另一支试管中产生黄色沉淀,则AgCl溶解度大于AgI |

室温下,相关沉淀物的溶度积常数(Ksp)如表:
沉淀物 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 | MnS |
Ksp | 8×10-16 | 4×10-32 | 4×10-14 | 4×10-13 |
下列说法不正确的是( )
CH3COOAg | AgCl | Ag2CrO4 | Ag2S | |
Ksp | 2.3×10-3 | 1.77×10-10 | 1.12×10-12 | 6.7×10-15 |
下列说法正确的是( )
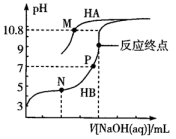
已知:M点溶液中c(A-)=c(HA)


已知:常温下,H3PO4的Ka1、Ka2、Ka3依次为7.1×10-3、6.2×10-8、4.5×10-13;H2C2O4的Ka1、Ka2依次为5.6×10-2、5.4×10-5 。
下列说法错误的是( )
①![]()
②![]()
常温下用0.1![]() 稀盐酸和0.1
稀盐酸和0.1![]()
![]() 溶液调节100
溶液调节100![]() 0.1
0.1![]() 的甘氨酸溶液的pH值,测得溶液pH值与甘氨酸的存在形式分布分数(α)如下图所示。
的甘氨酸溶液的pH值,测得溶液pH值与甘氨酸的存在形式分布分数(α)如下图所示。
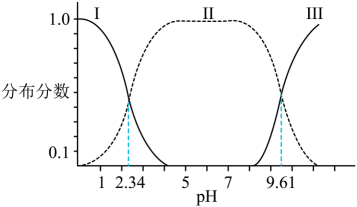
下列说法不正确的是