 点燃酒精灯
B .
点燃酒精灯
B . 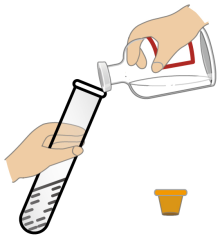 倾倒液体
C .
倾倒液体
C . 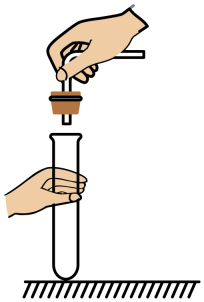 连接仪器
D .
连接仪器
D .  熄灭酒精灯
熄灭酒精灯

选项 | 实验目的 | 实验方案 |
A | 检验CH4中是否会有H2 | 点燃,在火焰上方罩一个干冷烧杯 |
B | 鉴别二氧化碳、氧气和空气 | 将燃着的木条分别伸入瓶中,观察现象 |
C | 分离KCl和MnO2的混合物 | 取样,加水溶解、过滤、洗涤、蒸发 |
D | 除去CO2中的少量CO | 将混合气体通过足量灼热的氧化铜 |
 B . 二氧化碳分子模型
B . 二氧化碳分子模型  C . 燃烧条件模型
C . 燃烧条件模型  D . 空气组成模型
D . 空气组成模型 
溶质 | 碘 | 高锰酸钾 | |||
溶剂 | 水 | 汽油 | 酒精 | 水 | 汽油 |
溶解性 | 微溶 | 易溶 | 可溶 | 易溶 | 不溶 |



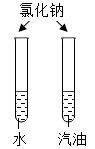 B . 探究可燃物燃烧的条件
B . 探究可燃物燃烧的条件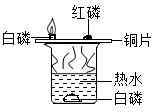 C . 探究铁生锈的条件
C . 探究铁生锈的条件 D . 探究二氧化碳和水的反应
D . 探究二氧化碳和水的反应





a.实验结束时应先熄灭B处酒精灯
b.C中增加的质量与B中固体减少的质量相等
c.反应结束后继续通入一氧化碳的目的是防止铜被氧化

用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。说明生成的气体是。
【查阅资料】
①
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
②四氧化三铁能与稀酸反应,但不产生气体。
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引。
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4:猜想二:剩余固体是。
【实验探究】
实验操作 | 实验现象及结论 |
【实验结论】铁和水蒸气反应的化学方程式为。
【反思与交流】该黑色固体不可能是Fe2O3 , 理由是。